题目内容
除去下列各物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 除杂试剂及操作方法 |
| A | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
| B | 氢气 | 氯化氢 | 依次通过足量的氢氧化钠溶液和浓硫酸 |
| C | 锌 | 铜 | 加入硫酸锌溶液,过滤 |
| D | 氧化钙 | 石灰石 | 高温煅烧 |
| A、A | B、B | C、C | D、D |
考点:物质除杂或净化的探究,常见气体的检验与除杂方法,金属的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:A、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
B、氯化氢能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸除去水蒸气,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、铜不能与硫酸锌溶液发生置换反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
D、石灰石高温煅烧生成氧化钙和二氧化碳,但无法除去石灰石中含有的杂质,故选项所采取的方法错误.
故选:B.
B、氯化氢能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸除去水蒸气,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、铜不能与硫酸锌溶液发生置换反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
D、石灰石高温煅烧生成氧化钙和二氧化碳,但无法除去石灰石中含有的杂质,故选项所采取的方法错误.
故选:B.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
除去下列各物质中混有的少量杂质,所用试剂不正确的是( )
| 序号 | 物质 | 杂质 | 所用试剂 |
| A | MnO2 | KCl | 水 |
| B | CO2 | H2O | 浓硫酸 |
| C | CaO | CaCO3 | 稀盐酸 |
| D | FeCl2 | CuCl2 | 铁屑 |
| A、A | B、B | C、C | D、D |
现代科技证明葡萄酒中含有的白藜芦醇具有美容养颜之功效.下列关于白藜芦醇(C14H12O3)的说法错误的是( )
| A、白藜芦醇由碳、氢、氧三种元素组成 |
| B、白藜芦醇中有29个原子 |
| C、白藜芦醇的相对分子质量为228 |
| D、白藜芦醇中碳、氢、氧三种元素的质量比为42:3:12 |
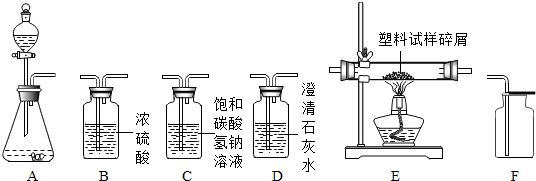
 多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问题:
多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问题: