题目内容
某同学发现他家菜园中蔬菜生长迟缓,便施用了一种氮肥,求:
(1)硝酸铵(NH4NO3)的相对分子质量是多少?
(2)计算硝酸铵中(NH4NO3)各元素的原子个数比.
(3)硝酸铵(NH4NO3)中各元素的质量比是多少?
(4)计算NH4NO3中氮元素的质量分数是多少?
(1)硝酸铵(NH4NO3)的相对分子质量是多少?
(2)计算硝酸铵中(NH4NO3)各元素的原子个数比.
(3)硝酸铵(NH4NO3)中各元素的质量比是多少?
(4)计算NH4NO3中氮元素的质量分数是多少?
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算
专题:化学式的计算
分析:(1)根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据一个硝酸铵分子的构成进行分析解答.
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据一个硝酸铵分子的构成进行分析解答.
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:(1)硝酸铵(NH4NO3)的相对分子质量是14+1×4+14+16×3=80.
(2)一个硝酸铵分子是由2个氮原子、4个氢原子、3个氧原子构成的,故硝酸铵中N、H、O三种元素的原子个数比为2:4:3.
(3)硝酸铵中氮、氢、氧元素的质量比为(14×2):(1×4):(16×3)=7:1:12.
(4)NH4NO3中氮元素的质量分数是
×100%=35%.
答:(1)硝酸铵(NH4NO3)的相对分子质量是80;
(2)硝酸铵中N、H、O三种元素的原子个数比2:4:3;
(3)硝酸铵中氮、氢、氧元素的质量比为7:1:12;
(4)NH4NO3中氮元素的质量分数是35%.
(2)一个硝酸铵分子是由2个氮原子、4个氢原子、3个氧原子构成的,故硝酸铵中N、H、O三种元素的原子个数比为2:4:3.
(3)硝酸铵中氮、氢、氧元素的质量比为(14×2):(1×4):(16×3)=7:1:12.
(4)NH4NO3中氮元素的质量分数是
| 14×2 |
| 80 |
答:(1)硝酸铵(NH4NO3)的相对分子质量是80;
(2)硝酸铵中N、H、O三种元素的原子个数比2:4:3;
(3)硝酸铵中氮、氢、氧元素的质量比为7:1:12;
(4)NH4NO3中氮元素的质量分数是35%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
推理是学习化学重要手段,下列推理正确的是( )
| A、点燃氢气前要检验其纯度,所以点燃其他可燃性气体前也要进行验纯 |
| B、氧气能支持燃烧,所以可以做燃料 |
| C、燃着的小木条伸入二氧化碳中,小木条熄灭,所以能使燃着小木条熄灭的一定是二氧化碳 |
| D、原子中有带电的粒子,所以整个原子是显电性的 |
二氧化碳和氢气可在一定条件下反应,生成一种重要的化工原料甲醇(CH3OH2):CO2+XH2
CH3OH+H2O.下列说法中不正确的是( )
| ||
| 加压 |
| A、X的数值为3 |
| B、属于化合反应 |
| C、钌一膦络合物的质量在反应前后一定不会变化 |
| D、为CO2的利用创造了一种新途径 |
已知两种不同原子,一种核内有8个质子,8个中子,另一种核内有8个质子,9个中子,则它们不相等的是( )
| A、核外电子数 | B、原子带电量 |
| C、核电荷数 | D、原子质量 |
实验室需收集一瓶约含四分之一空气的氧气,下列操作正确的是( )
A、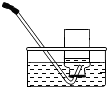 集气瓶中灌
| ||
B、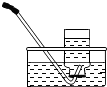 集气瓶中灌
| ||
C、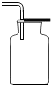 导管伸入到集气瓶体积的
| ||
D、 导管伸入到集 气瓶体积的
|
青篙素(化学式为C15H22O5)是治疗疟疾的特效药.关于青篙素的说法正确的是( )
| A、青篙素属于氧化物 |
| B、28.2g青篙素中含碳元素的质量为18g |
| C、一个青篙素分子含有11个氢分子 |
| D、C、H、O 三种元素的质量比为 15:22:5 |
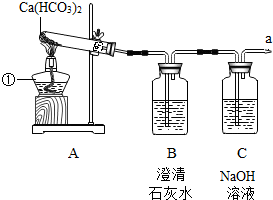 我市不少人发现浴室喷头的使用很容易出现白色固体附着,这是因为我市属于石灰岩地区,水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成难溶性的盐、气体等物质.某小组探究碳酸氢钙受热分解后产物的成分.
我市不少人发现浴室喷头的使用很容易出现白色固体附着,这是因为我市属于石灰岩地区,水中含有较多的可溶性的钙、镁化合物,其中碳酸氢钙[Ca(HCO3)2]受热易分解,生成难溶性的盐、气体等物质.某小组探究碳酸氢钙受热分解后产物的成分.