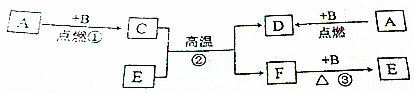
题目内容
8.下列四个实验是判断稀硫酸与NaOH、NaCl、Na2CO3、Ba(NO3)2溶液能否发生复分解反应:A.H2SO4+NaOH B.H2SO4+NaCl C.H2SO4+Na2CO3 D.H2SO4+Ba(NO3)2.(1)复分解反应发生的条件是有沉淀、气体或是水生成;
(2)能反应,但没有明显现象的是A(填序号);
(3)实验D中发生的反应可用化学方程式表示为H2SO4+Ba(NO3)2═2HNO3+BaSO4↓;
(4)同学们将实验后所有物质倒入同一烧杯中,后续实验及现象如图:
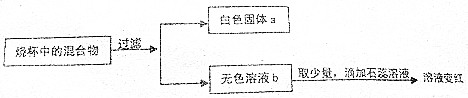
综合分析有关实验的现象回答问题.
①白色固体a中含有的物质是硫酸钡;
②无色溶液b中一定含有的阴离子是SO42-、NO3-、Cl-.
分析 根据复分解反应的条件以及物质的性质和化学方程式的书写进行分析解答即可.
解答 解:(1)复分解反应发生的条件是有沉淀、气体或是水生成,故填:有沉淀、气体或是水生成;
(2)硫酸和氢氧化钠能反应,但没有明显现象,故填:A;
(3)实验D中硫酸和硝酸钡能反应生成硝酸和硫酸钡,故填:H2SO4+Ba(NO3)2═2HNO3+BaSO4↓;
(4)氢氧化钠能与硫酸反应生成硫酸钠和水,硫酸和氯化钠不反应,硫酸和硝酸钡能反应生成硝酸和硫酸钡,故得到的暴色沉淀a是硫酸钡,得到的无色溶液能使石蕊试液变红,故一定含有硫酸,一定含有硫酸根离子,一定含有氯离子和硝酸根离子,故填:硫酸钡;SO42-、NO3-、Cl-.
点评 本题考查的是复分解反应的条件以及物质的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20.某同学认真分析“自然界中的氧循环”图后,产生了下列想法,其中一定错误的是( )
| A. | 动植物呼吸和燃料燃烧过程中都发生了有氧气参与的化学变化 | |
| B. | 森林里空气的氧含量高于沙漠中的空气 | |
| C. | 教室中的某个氧原子有可能来自上世纪的欧洲田园 | |
| D. | 绿色植物的作用是使自然界中的氧原子总数增加 |
18.下列化肥灼烧时可以燃烧,加熟石灰又放出有刺激性气味氨气的是 ( )
| A. | 氨水 | B. | 硝酸铵 | C. | 磷酸钙 | D. | 硫酸钾 |
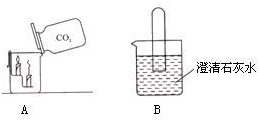
 农村广泛采用塑料大棚种植蔬菜,为了提高蔬菜的产量,常在塑料大棚中补充二氧化碳作为气体肥料,农业科技人员根据蔬菜的品种和大棚的容积,建议某蔬菜大棚每天一次性补充1.76kg二氧化碳气体,他们利用自家储备的碳酸氢铵化肥(如图所示)和工业上的废稀硝酸反应产生二氧化碳气体,反应的化学方程式为;NH4HCO3+HNO3═NH4NO3+H2O+CO2↑.
农村广泛采用塑料大棚种植蔬菜,为了提高蔬菜的产量,常在塑料大棚中补充二氧化碳作为气体肥料,农业科技人员根据蔬菜的品种和大棚的容积,建议某蔬菜大棚每天一次性补充1.76kg二氧化碳气体,他们利用自家储备的碳酸氢铵化肥(如图所示)和工业上的废稀硝酸反应产生二氧化碳气体,反应的化学方程式为;NH4HCO3+HNO3═NH4NO3+H2O+CO2↑.