题目内容
1.根据如图回答下面试验中的问题:
(1)装置甲可将硬水软化,该实验操作叫做蒸馏.
(2)实验乙中可观察到的主要现象是发出明亮的蓝紫色火焰,生成刺激性气味的气体,放出大量的热,如果瓶内的液体是氢氧化钠溶液,其发生反应的化学方程式是2NaOH+SO2=Na2SO3+H2O.
(3)实验丙可以证明燃烧的条件:证明燃烧需要温度达到着火点的现象是试管中的白磷燃烧而红磷没有燃烧.和丁相比该实验设计中有一个很明确的优点,它是防止污染空气.
分析 (1)根据装置I所表示的净水操作的名称是蒸馏进行分析;
(2)根据硫燃烧的现象以及碱的性质进行分析;
(3)根据燃烧的条件以及装置特点进行分析.
解答 解:(1)装置I所表示的净水操作的名称是蒸馏,故填:蒸馏;
(2)硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成刺激性气味的气体,放出大量的热,生成的二氧化硫与氢氧化钠反应生成亚硫酸钠和水,故填:发出明亮的蓝紫色火焰,生成刺激性气味的气体,放出大量的热;2NaOH+SO2=Na2SO3+H2O;
(3)试管中的白磷燃烧而红磷没有燃烧,证明了可燃物燃烧,温度需要达到其着火点;和丁相比该实验设计中有一个很明确的优点,反应是在密闭容器内进行的,避免了空气的污染;故填:试管中的白磷燃烧而红磷没有燃烧;防止污染空气.
点评 本题难度不大,考查蒸馏、燃烧等实验,熟悉常见的实验是解答的关键.

练习册系列答案
相关题目
11.下列实验现象正确的是( )
| A. | 打开浓硫酸瓶盖,产生白雾 | |
| B. | 铁丝在氧气中燃烧发出耀眼的白光 | |
| C. | 淀粉中加入碘酒混合物变蓝色 | |
| D. | 硝酸铵固体溶于水中,溶液温度升高 |
9.下列对一些事实的解释中合理的是( )
| 现象 | 解释 | |
| A | 氢氧化钠溶液、氢氧化钾溶液都显碱性 | 两种溶液中都含有大量的OH- |
| B | 浓硫酸敞口放置于空气中会变稀 | 硫酸分子运动到空气中 |
| C | 氯化钠溶液能导电 | 溶液中含有自由移动的电子 |
| D | 金刚石、石墨物理性质差异很大 | 碳原子结构不同 |
| A. | A | B. | B | C. | C | D. | D |
6.CO2是重要的资源,以其为原料可获得下列四种物质.下列说法错误的是( )
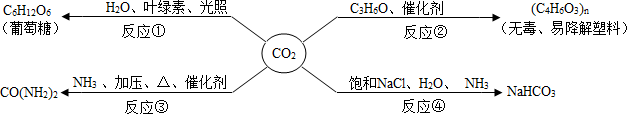

| A. | 反应①是太阳能转化为化学能 | |
| B. | 反应②的实现有利于缓解“白色污染” | |
| C. | 反应③是化合反应 | |
| D. | 反应④获得产品后的剩余液中,溶质只有NH4Cl |
3.下列推理正确的是( )
| A. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的物质一定是化合物 | |
| B. | 碱溶液一定能使酚酞试剂变红,能使酚酞试剂变红的一定是碱溶液 | |
| C. | 分子、原子都是不带电的粒子,但是不带电的粒子不一定是分子、原子 | |
| D. | 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应 |
 A、B、C、D、E均为初中化学常见的化合物.其中A、B、C均含同一种金属元素,C可用于改良酸性土壤,D的溶液呈蓝色,E是一种常见的酸.它们之间存在如图所示的转化关系(“一”表示相互间能反应,“→”表示在某种条件下能生成该物质,部分反应物和生成物已略去). 请回答下列问题.
A、B、C、D、E均为初中化学常见的化合物.其中A、B、C均含同一种金属元素,C可用于改良酸性土壤,D的溶液呈蓝色,E是一种常见的酸.它们之间存在如图所示的转化关系(“一”表示相互间能反应,“→”表示在某种条件下能生成该物质,部分反应物和生成物已略去). 请回答下列问题.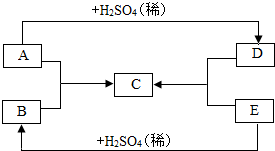 A、B、C、D为初中化学常是的物质,它们之间存在如下图所示的转化关系.已知
A、B、C、D为初中化学常是的物质,它们之间存在如下图所示的转化关系.已知 如图是初中化学中几种常见物质间的反应及转化关系,C可作温室气料,E是胃液中含有的酸,F俗称苏打.图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质.
如图是初中化学中几种常见物质间的反应及转化关系,C可作温室气料,E是胃液中含有的酸,F俗称苏打.图中“-”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质.