题目内容
12.春节期间小明对当地雨水的酸碱度进行了检测.他将收集的雨水,每隔5min用pH计检测一次,其pH值如表.| 测定时间 | 8:05 | 8:10 | 8:15 | 8:20 | 8:25 | 8:30 |
| pH | 4.94 | 4.92 | 4.90 | 4.88 | 4.86 | 4.85 |
(2)经调查,近几天空气中SO2、NO2含量明显增多,小明很那纳闷;春节期间,工厂大多停产、运输车辆也比往日减少,空气中SO2、NO2怎么会增多呢?耳边鸣响的鞭炮声使他恍然大悟,鞭炮爆炸会产生SO2、NO2等污染物,小明通过查询资料得知,SO2(含NO2)的化学性质与CO2相似.他设计用氢氧化钠溶液来吸收鞭炮爆炸时产生的SO2(含NO2),情写出有关的化学方程式SO2+2NaOH═Na2SO3+H2O.
(3)通过小明的实验,你作为一名有一定科学素养的中学生,如何看待燃放鞭炮这一现象?
分析 (1)根据二氧化碳和水反应,生成碳酸解答;pH<5.6的雨水称为酸雨,根据题中信息解答;当溶液的pH<7时,随着pH的减小酸性增强;
(2)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(3)根据烟花燃放可能造成的污染有:大气污染、固体废弃物污染、噪音污染等解答;
解答 解:
(1)二氧化碳和水反应,生成碳酸,反应的化学方程式为:CO2++H2O=H2CO3;雨水的pH小于5.6,属于酸雨,在测定的期间,雨水水样的pH逐渐减小,酸性增强.
(2)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O.
(3)烟花燃放可能造成的污染有:大气污染、固体废弃物污染、噪音污染等;禁止燃放烟花爆竹,是防止环境污染的一项重要措施,我们应加强环保意识.
答案:
(1)CO2++H2O=H2CO3 ;是;增强;
(2)SO2+2NaOH═Na2SO3+H2O;
(3)烟花燃放可能造成的污染有:大气污染、固体废弃物污染、噪音污染等;
点评 解答本题要掌握化学方程式的书写方法以及形成酸雨的条件等方面的知识,只有这样才能对相关方面的问题做出增强的判断.

练习册系列答案
相关题目
2.假设有(1)Fe、CuSO4、稀H2SO4;(2)CuSO4、KOH、稀HCl;(3)Mg、稀HCl、NaOH;(4)Na2CO3、稀H2SO4、CaCl2四组物质,将它们分别同时放入足量水中,经充分搅拌后静置观察.下列同学们讨论的发言中,正确的有( )
| A. | 只有(1)组液体中,一定有不溶物生成 | |
| B. | 只有(1)、(2)组溶液呈蓝色,且一定有沉淀出现 | |
| C. | 只有(2)、(4)组液体中,不可能出现浑浊 | |
| D. | 四组液体中一定都会出现沉淀 |
3.铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如表.请计算:
(1)合金中铜、镁的质量比33:17.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
20.下列事故的处理错误的是( )
| A. | 如果不慎将浓硫酸沾在皮肤上,应立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液 | |
| B. | 如果不小心将酒精灯打翻而造成酒精在桌面上燃烧起来,应立即用湿抹布扑盖 | |
| C. | 如果不慎将氢氧化钠溶液沾在皮肤上,应立即用大量的水冲洗,再涂上硼酸溶液 | |
| D. | 如果因胃酸过多而引起的胃不适,可以喝一些稀氢氧化钠溶液加以中和 |
7.实验操作先后顺序正确的是( )
| A. | 蒸发食盐水时,先在铁圈上放置蒸发皿,后放酒精灯 | |
| B. | 测定溶液pH,先将试纸湿润,后用干净的玻璃棒蘸取待测液滴在试纸上 | |
| C. | 实验室用加热高锰酸钾并用排水法收集氧气时,实验结束前先熄灭酒精灯,后把导管从水槽中取出 | |
| D. | 如果不慎将氢氧化钠沾到皮肤上,先用大量的水冲洗,后涂上硼酸溶液 |
17. 某校学习小组准备探究气体的测定和数据处理方法.
某校学习小组准备探究气体的测定和数据处理方法.
【提出问题】
如何利用石灰石(主要成分为CaC03)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
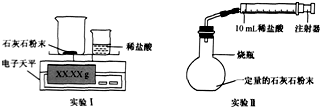
【实验设计】通过下列两个实验分别测定C02的质量和体积.
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaC03完全反应的实验现象是最后一次加稀盐酸后,无气泡冒出;
(2)实验Ⅱ中,先连接好装置并检查气密性,然后装好药品,最后将10mL稀盐酸快速推入烧瓶中.若稀盐酸是分几次缓慢推入的,则可能造成的后果是由于反应生成气体使装置中压强增大,再次推入较困难;
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯十石灰石粉末)+m(小烧杯十稀盐酸)],要计算生成C02的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯十反应后剩余物)
(4)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定):
根据以上实验过程和数据综合分析,最终生成C02的体积80 mL.
(5)该学习小组的同学采集了一块石灰石样品,将其敲碎后,称出6g放入烧杯内(烧杯质量为20g).然后加入50g稀盐酸(足量),充分反应后,再称量为73.8g(连烧杯一起).试回答:
①将石灰石样品敲碎的主要目的是增大反应物的接触面积,使反应更充分.
②该实验过程中,共产生CO2的质量2.2g.
③该石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留一位小数)
 某校学习小组准备探究气体的测定和数据处理方法.
某校学习小组准备探究气体的测定和数据处理方法.【提出问题】
如何利用石灰石(主要成分为CaC03)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定C02的质量和体积.
【分析与表达】
(1)实验I中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaC03完全反应的实验现象是最后一次加稀盐酸后,无气泡冒出;
(2)实验Ⅱ中,先连接好装置并检查气密性,然后装好药品,最后将10mL稀盐酸快速推入烧瓶中.若稀盐酸是分几次缓慢推入的,则可能造成的后果是由于反应生成气体使装置中压强增大,再次推入较困难;
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯十石灰石粉末)+m(小烧杯十稀盐酸)],要计算生成C02的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯十反应后剩余物)
(4)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
(5)该学习小组的同学采集了一块石灰石样品,将其敲碎后,称出6g放入烧杯内(烧杯质量为20g).然后加入50g稀盐酸(足量),充分反应后,再称量为73.8g(连烧杯一起).试回答:
①将石灰石样品敲碎的主要目的是增大反应物的接触面积,使反应更充分.
②该实验过程中,共产生CO2的质量2.2g.
③该石灰石样品中碳酸钙的质量分数是多少?(写出计算过程,结果保留一位小数)
1.日常生活中的下列物质,属于有机合成材料的是( )
| A. | 铝合金 | B. | 玻璃 | C. | 橡胶轮胎 | D. | 钢筋混凝土 |
