题目内容
18.氢气是一种热值高的清洁能源,也是重要的化工原料.(1)写出在加热条件下,H2与二氧化锗(CeO2)反应制备金属锗的化学方程式:GeO2+2H2$\frac{\underline{\;\;△\;\;}}{\;}$Ge+2H2O.
(2)如何大量、廉价地制备氢气是各国正努力研究的课题.日本科学家最近开发出一种含镍氧化物半导体粉末,将少量这种粉末放入水中,用波长为402nm的可见光照射,能够不断地将水分解成氢气和氧气.在上述过程中,这种氧化物粉末的作用是催化作用;写出该反应的化学方程式2H2O$\frac{\underline{\;含镍氧化物\;}}{可见光}$2H2↑+O2↑.
分析 (1)在加热条件下,H2与二氧化锗(CeO2)反应生成锗和水,写出反应的化学方程式即可.
(2)根据题意,一种含镍氧化物半导体粉末,将少量这种粉末放入水中,用波长为402nm的可见光照射,能够不断地将水分解成氢气和氧气,进行分析解答.
解答 解:(1)在加热条件下,H2与二氧化锗(CeO2)反应生成锗和水,反应的化学方程式为:GeO2+2H2$\frac{\underline{\;\;△\;\;}}{\;}$Ge+2H2O.
(2)一种含镍氧化物半导体粉末,将少量这种粉末放入水中,用波长为402nm的可见光照射,能够不断地将水分解成氢气和氧气,这种氧化物粉末的作用是催化作用,
故答案为:(1)GeO2+2H2$\frac{\underline{\;\;△\;\;}}{\;}$Ge+2H2O;(2)催化作用;2H2O$\frac{\underline{\;含镍氧化物\;}}{可见光}$2H2↑+O2↑.
点评 本题难度不大,掌握氢气的化学性质、化学方程式的书写方法并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
8.下列变化中,既有物理变化又有化学变化的是( )
| A. | 从矿山中开采铁矿石再将铁矿石磨成粉末 | |
| B. | 点燃酒精灯时,酒精沿着纱条向上,然后在灯芯处汽化燃烧 | |
| C. | 钢钉压成钢条,钢条拉成钢丝,钢丝结成钢丝网 | |
| D. | 冰融化成水,水加热变为水蒸气 |
6.日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
| A. | 用汽油洗去手上的油污 | B. | 用洗发精洗去头发上的油脂 | ||
| C. | 用洗面奶洗去皮肤上的油脂 | D. | 用洗洁精洗去餐具上的油污 |
7.受北方强冷空气影响,甘肃省曾出现了大范围的沙尘天气过程.这次沙尘天气过程中,有些地方的能见度一度降至零.沙尘暴天气使空气中增加了大量的( )
| A. | 可吸入颗粒物 | B. | 一氧化碳 | C. | 二氧化氮 | D. | 二氧化硫 |
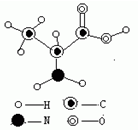 自然界生命体的有机物组成除C、H、O外还有其他元素,如藻类物质(化学式可表示为C106H263O110N16P)的组成中就含有N和P.α-丙氨酸是组成人体蛋白质的氨基酸之一,其分子结构如图所示:
自然界生命体的有机物组成除C、H、O外还有其他元素,如藻类物质(化学式可表示为C106H263O110N16P)的组成中就含有N和P.α-丙氨酸是组成人体蛋白质的氨基酸之一,其分子结构如图所示: