题目内容
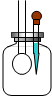 探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,集气瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,集气瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )| 组合 | 滴 管 中 | 集气瓶中 |
| A | Ca(OH)2 | HCl(气) |
| B | HCl | Zn(固) |
| C | NaOH | CO2(气) |
| D | H2SO4(浓) | H2O(液) |
| A、A | B、B | C、C | D、D |
考点:反应现象和本质的联系,浓硫酸的性质及浓硫酸的稀释,酸的化学性质,碱的化学性质
专题:常见的酸 酸的通性,常见的碱 碱的通性
分析:分析装置的原理:要使气球变大就要使瓶中的气体减少或瓶中温度降低.可以根据物质之间混合时的反应特点方面进行分析、判断.
解答:解;A、氯化氢气体和氢氧化钙溶液反应生成氯化钙和水,集气瓶内的压强变小,气球变大,故A符合题意;
B、稀盐酸和锌反应生成氢气,集气瓶内的压强变大,气球变小,故B不符合题意;
C、二氧化碳和氢氧化钠溶液发生反应生成碳酸钠和水,集气瓶内的压强变小,气球变大,故C符合题意;
D、浓硫酸溶于水放热,温度升高,集气瓶内的压强变大,气球变小,故D不符合题意.
故选AC.
B、稀盐酸和锌反应生成氢气,集气瓶内的压强变大,气球变小,故B不符合题意;
C、二氧化碳和氢氧化钠溶液发生反应生成碳酸钠和水,集气瓶内的压强变小,气球变大,故C符合题意;
D、浓硫酸溶于水放热,温度升高,集气瓶内的压强变大,气球变小,故D不符合题意.
故选AC.
点评:本题主要考查了酸、碱、盐的化学性质,解此类题的关键是分析装置的原理,再根据酸、碱、盐的性质判断物质间反应时是否有气体生成或气体参加反应.

练习册系列答案
相关题目
掌握物质的分类是学好化学的基础,指出下列物质中属于碱的是( )
| A、Na2CO3 |
| B、KOH |
| C、MgO |
| D、Cu |
某反应的微观示意图如图(一种小球代表一种元素的原子),下列说法错误的是( )

| A、该反应中共有三种元素 |
| B、图中反应物都是化合物 |
| C、该反应的本质是原子的重新组合 |
| D、该反应前后分子的种类发生改变 |
在托盘天平的两个烧杯中放入相同质量的过量的HCl,使天平平衡,在左盘放入5.6克CaO,为了使天平平衡,在右盘加入CaCO3的质量( )
| A、10克 | B、14.4克 |
| C、5.6克 | D、4.4克 |
不法分子常常用金光闪闪的“金元宝”(铜锌合金)来蒙骗人们,下列鉴别方法中错误的是( )
| A、加盐酸 | B、测密度 |
| C、看颜色 | D、用火烧 |


 如图所示,在一个具有刻度和可以左右滑动的活塞的玻璃容器里放入白磷(足量),把密封管内的容积分为5等份.将玻璃容器固定好(见图,固定装置已省略),将玻璃容器固定在盛有80℃热水(恒温)的烧杯上,(白磷燃烧所需的最低温度为40℃)进行实验.试回答:
如图所示,在一个具有刻度和可以左右滑动的活塞的玻璃容器里放入白磷(足量),把密封管内的容积分为5等份.将玻璃容器固定好(见图,固定装置已省略),将玻璃容器固定在盛有80℃热水(恒温)的烧杯上,(白磷燃烧所需的最低温度为40℃)进行实验.试回答: