题目内容
2.水是生命之源,也是人类最宝贵的资源.用学过的化学知识回答下列问题:(1)自然界中的水都不是纯水,通常用煮沸的方法使硬水软化,主要目的是除去了水中过多的Ca2+、Mg2+(填离子符号).
(2)洗碗时,用水很难洗去油渍,但能用洗涤剂就能轻松洗去,请你说出洗涤剂具有 的作用是乳化作用.
(3)自来水的净化中,常用漂白粉来消毒杀菌,其有效成分为次氯酸钙Ca(ClO)2,其中氯元素的化合价为 +1,其制作原理为2Cl2+2Ca(OH)2═Ca(ClO)2+M+2H2O,则M的化学式为CaCl2.
分析 (1)根据硬水和软水的区别以及硬水的软化方法分析;
(2)根据洗洁精具有乳化作用分析.
(3)根据化学反应前后各元素的原子个数不变,在化合物中,各元素正负化合价的代数和为零分析回答.
解答 解:(1)硬水和软水的区别在于所含的钙、镁离子的多少,自然界中的水都不是纯水,通常用煮沸的方法使硬水软化,主要目的是除去了水中过多的Ca2+、Mg2+;由于活性炭具吸附性,生活用水在净化过程中常用活性炭吸附色素和异味;
(2)用洗洁精清洗油污,是利用了洗洁精的乳化作用.
(3)在次氯酸钙中,钙元素是+2价,氧元素是-2价,设氯元素的化合价为x,则有(+2)+2x+(-2)×2=0,解得x=+1,
在2Cl2+2Ca(OH)2═Ca(ClO)2+M+2H2O中,反应前含有2个Ca,4个Cl,4个O,4个H,反应后含有1个Ca,2个Cl,4个O,4个H,1个C,故1个M中含有1个Ca,2个Cl,是氯化钙.
故答案为:(1)Ca2+、Mg2+ (2)乳化作用 (3)+1,CaCl2
点评 掌握常见的水的净化的方法和质量守恒定律以及化合价规则是解答本题的关键.化学源于生活,生活中蕴含着许多化学知识,学好化学知识,解决好生活中的一些问题.

练习册系列答案
相关题目
1.下列反应的化学方程式书写正确的是( )
| A. | 2H2O═2H2↑+O2↑ | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | 2Cu+O2?2CuO | D. | NH4Cl+AgNO3═AgCl+NH4NO3 |
10.如图是某反应的微观示意图,以下说法正确的是( )

| A. | 分子是化学变化中最小粒子 | |
| B. | 如图表示的微观变化过程中共有三种分子 | |
| C. | 该反应有单质生成 | |
| D. | 参加反应的“ ”分子与“ ”分子与“ ”分子的个数比为1:3 ”分子的个数比为1:3 |
17.下列实验中与如图相符合的是( )
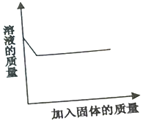

| A. | 向稀盐酸中加入碳酸钾粉末 | |
| B. | 向稀硫酸中加入镁条 | |
| C. | 向硝酸银溶液中加入铜粉 | |
| D. | 向不饱和硝酸钾溶液加入硝酸钾晶体 |
7.X、Y、Z三种元素的化合价分别为+1,+7,-2,则这三种元素所组成的化合物的化学式可能为( )
| A. | XYZ | B. | X2YZ4 | C. | XYZ4 | D. | X2YZ3 |
14.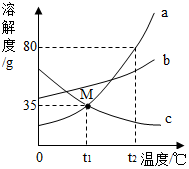 如图是不含结晶水的A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的A、B、C三种物质的溶解度曲线,下列说法正确的是( )
 如图是不含结晶水的A、B、C三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的A、B、C三种物质的溶解度曲线,下列说法正确的是( )| A. | M点表示A、C两种物质的饱和溶液质量相等 | |
| B. | t2℃时、将50 g A物质加入50 g水中充分搅拌,得到100 g A的饱和溶液 | |
| C. | 将三种物质的饱和溶液从t2℃降至t1℃,溶质质量分数最小的一定是C | |
| D. | 将t2℃时A、B两种物质的饱和溶液降温到t1℃时,析出晶体的质量:A<B |
11.分类法是化学学习的重要方法,下列说法正确的是( )
| A. | 生石灰、纯碱、浓硫酸都可以用作干燥剂 | |
| B. | 铁、锌、碘元素都属于人体必需微量元素 | |
| C. | 硫离子的核外电子数为16 | |
| D. | KNO3、CO(NH2)2、NH4H2PO4都属于复合肥料 |
12.下列物质中属于纯净物的是( )
| A. | 食醋 | B. | 白酒 | C. | 大理石 | D. | 生石灰 |