题目内容
9.为了测定某品牌小苏打样品中碳酸氢钠的质量分数,向10g小苏打样品加入足量稀盐酸,充分反应后,放出4.4g二氧化碳气体.假设该样品中只含有氯化钠一种杂质,请计算(1)样品中碳酸氢钠的质量
(2)样品中氯化钠的质量分数.
分析 根据质量守恒定律,化学反应前后物质的总质量不变,据此可以求出二氧化碳的质量,然后根据反应的化学方程式,利用二氧化碳的质量进行求算,据此解答即可.
解答 解:设碳酸氢钠的质量为x
NaHCO3+HCl=NaCl+H2O+CO2↑
84 44
x 4.4g
$\frac{84}{x}$=$\frac{44}{4.4g}$
x=8.4g
所以氯化钠的质量分数为:$\frac{10g-8.4g}{10g}$×100%=16%.
故答案为:(1)样品中碳酸氢钠的质量为8.4g;
(2)样品中氯化钠的质量分数为16%.
点评 本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式结合题干提供的数据进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
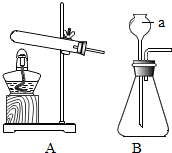
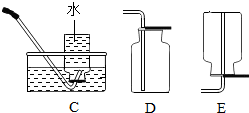
19.如图为实验室制取气体的常用装置.
(1)仪器a的名称是分液漏斗.
(2)用A装置作加热高锰酸钾制取氧气的发生装置,明显存在的不足是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取二氧化碳应选择的发生装置是B.
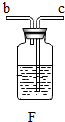
(4)实验室为得到干燥的O2,可将制得的气体从导管b通入装有浓硫酸溶液的F装置中,除去水蒸气.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)用A装置作加热高锰酸钾制取氧气的发生装置,明显存在的不足是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取二氧化碳应选择的发生装置是B.
(4)实验室为得到干燥的O2,可将制得的气体从导管b通入装有浓硫酸溶液的F装置中,除去水蒸气.
17.七氧化二锰常用于测定矿石铁的含量,其中七氧化二锰元素的化合价为( )
| A. | -1 | B. | +3 | C. | +5 | D. | +7 |
4.下列实验操作正确的是( )
| A. |  量取3.5mL液体 | B. |  甲烷验纯 | C. | 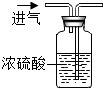 干燥二氧化碳 | D. |  测定溶液pH |
14.下列化学用语表达的意义正确的是( )
| A. | 3H:3个氢分子 | B. | Mg+2:+2价镁离子 | C. | Fe3+:铁离子 | D. | N2:2个氦原子 |
1.下列离子能在pH=2的水溶液中大量共存的是( )
| A. | Cl-、NO3-、K+、Na+ | B. | HCO3-、Cl-、SO42-、Na+ | ||
| C. | SO42-、NO3-、K+、OH- | D. | NH4+、Cl-、OH-、K+ |
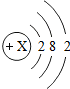 结合如图回答下列问题
结合如图回答下列问题 根据如图标签上的信息填空.
根据如图标签上的信息填空.