题目内容
金属材料在生产、生活中的应用非常广泛.
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的 (填序号).
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的氧气、 等发生化学反应的过程.
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 .
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是 、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和 .
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(5)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图所示装置进行实验:实验中玻璃管内的粉末由 色变黑色.
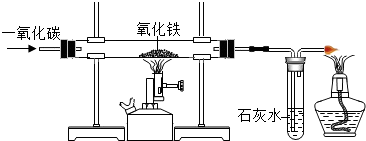
(6)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁 t.(计算结果保留1位小数)
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的氧气、
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是
②方法二所选用的3种物质是锌片、铜片和
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(5)炼铁的原理是利用一氧化碳与氧化铁反应.在实验室里,可用如图所示装置进行实验:实验中玻璃管内的粉末由

(6)某钢铁厂每天需消耗5000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁
考点:金属的物理性质及用途,金属活动性顺序及其应用,含杂质物质的化学反应的有关计算,金属锈蚀的条件及其防护,金属资源的保护
专题:金属与金属材料
分析:(1)根据铜合金的导热性分析;
(2)根据铁制品锈蚀的条件进行解答;
(3)根据金属的回收利用的目的解答,回收金属就是为了节约金属资源.
(4)在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸反应生成氢气.
(5)根据已有的知识进行分析,一氧化碳能与氧化铁反应生成铁和二氧化碳,氧化铁为红色,铁粉为黑色.
(6)由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
(2)根据铁制品锈蚀的条件进行解答;
(3)根据金属的回收利用的目的解答,回收金属就是为了节约金属资源.
(4)在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸反应生成氢气.
(5)根据已有的知识进行分析,一氧化碳能与氧化铁反应生成铁和二氧化碳,氧化铁为红色,铁粉为黑色.
(6)由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答:解:(1)火锅的锅体是由铜合金制造的,主要是因为铜合金具有很好的导热性;
(2)铁制品锈蚀的条件:铁与空气中的氧气、水等发生的化学反应;
(3)回收利用金属是为了节约金属资源.
(4))①可以选用的另外一种药品是铁片,铁不与硫酸锌溶液反应,说明锌在铁的前面,铁能与硫酸铜溶液反应,说明铁在铜的前面;
②可以选用的另外一种药品是硫酸亚铁溶液,锌能与硫酸亚铁反应,说明锌在铁的前面,铜不与硫酸亚铁反应,说明铁在铜的前面;
(5)红色的氧化铁粉末被还原为黑色的铁粉,一氧化碳与氧化铁反应生成铁和二氧化碳.
(6)解:设理论上可炼出含铁98%的生铁质量为x.
Fe2O3+3CO
2Fe+3CO2
160 112
5000t×80% 98%x
=
x≈2857.1t
答:该钢铁厂理论上可日产含Fe98%的生铁质量是2857.1t
故答案为:(1)B;(2)水(3)A(4)铁片,硫酸亚铁(5)红(6)2857.1
(2)铁制品锈蚀的条件:铁与空气中的氧气、水等发生的化学反应;
(3)回收利用金属是为了节约金属资源.
(4))①可以选用的另外一种药品是铁片,铁不与硫酸锌溶液反应,说明锌在铁的前面,铁能与硫酸铜溶液反应,说明铁在铜的前面;
②可以选用的另外一种药品是硫酸亚铁溶液,锌能与硫酸亚铁反应,说明锌在铁的前面,铜不与硫酸亚铁反应,说明铁在铜的前面;
(5)红色的氧化铁粉末被还原为黑色的铁粉,一氧化碳与氧化铁反应生成铁和二氧化碳.
(6)解:设理论上可炼出含铁98%的生铁质量为x.
Fe2O3+3CO
| ||
160 112
5000t×80% 98%x
| 160 |
| 112 |
| 4000t |
| 98%x |
答:该钢铁厂理论上可日产含Fe98%的生铁质量是2857.1t
故答案为:(1)B;(2)水(3)A(4)铁片,硫酸亚铁(5)红(6)2857.1
点评:化学来源于生产生活,也服务于生产生活,因此在近年的中考中,与生产生活实际相关的情景题已渐渐成为亮点

练习册系列答案
相关题目
下列有关物质的检验方法和结论都正确的是( )
| A、经点燃,产生蓝色火焰的气体一定是一氧化碳 |
| B、向某无色溶液中滴入酚酞试液,溶液变红色,该溶液一定是碱溶液 |
| C、向某无色溶液中滴入盐酸,无明显现象,再滴入氯化钡溶液,产生白色沉淀,该溶液中一定含有硫酸根离子 |
| D、把燃着的木条伸入某无色气体中,木条熄灭,该气体一定是二氧化碳 |
在天平两端各放一只盛有100克,4.9%稀硫酸的烧杯,调节天平平衡,向左盘的烧杯中加入2.4克镁,充分反应后,下列操作有可能使天平平衡的是( )
| A、向右拨动游码至2.2克 |
| B、向右盘中加入2.4克铝和铁的混合物 |
| C、向右盘中加入2.4克铝 |
| D、向右盘中加入4.2克碳酸镁和碳酸钠的混合物 |


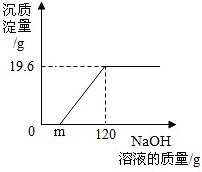 某炼铜厂排放的废水中含有硫酸和硫酸铜两种污染物,取废水400g,向其中加入溶质质量分数为20%的氢氧化钠溶液.测得质量关系如图:
某炼铜厂排放的废水中含有硫酸和硫酸铜两种污染物,取废水400g,向其中加入溶质质量分数为20%的氢氧化钠溶液.测得质量关系如图: