题目内容
14. NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:
NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:(1)由图可知,20℃时氯化钠的溶解度为36g.
(2)依据图分析下列问题:50℃时,将氯化钠、硝酸钾固体各40g 分别加入两只各盛有100g水的烧杯中,充分搅拌,其中NaCl(填写物质化学式)得到饱和溶液;另一种物质的溶液中再加 入45.5g该溶质,溶液恰好饱和;若将温度都降到20℃,硝酸 钾溶液中溶质的质量分数<(填“>”“<”或“=”)氯化钠溶液中溶质的质量分数.
分析 (1)根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小;
(2)根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液是否饱和;
饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
解答 解:(1)由图一可知,20℃时氯化钠的溶解度为36g.
(2)50℃时,氯化钠的溶解度是37g,硝酸钾的溶解度是85.5g,将氯化钠、硝酸钾固体各40g分别加入两只各盛有100g水的烧杯中,充分搅拌,其中NaCl得到饱和溶液;另一种物质的溶液中再加入45.5g该溶质,溶液恰好饱和;若将温度都降到20℃,氯化钠和硝酸钾都仍然是饱和溶液,硝酸钾的溶解度小于氯化钠的溶解度,因此硝酸钾溶液中溶质的质量分数<氯化钠溶液中溶质的质量分数.
故填:<.
(1)36;
(2)NaCl、45.5g、<.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.一种奇妙的蜡烛,点燃后怎么吹也吹不灭,它看上去和普通蜡烛一样,究竟是什么原因能让蜡烛持续燃烧呢?
【查阅资料】普通蜡烛右石蜡和烛芯制成,吹不灭的蜡烛是在烛芯上包裹一层一种金属与少量稀土元素形成的合金粉末,着火点为150℃,蜡烛燃烧时,烛芯里的金属不燃烧;蜡烛一熄灭,末降温的金属就燃烧起来,从而再将蜡烛引燃.
【思考与解释】蜡烛燃烧时,烛芯里的金属为什么不燃烧?蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以燃烧.
【实验探究】小莺通过查阅资料已知吹不灭的蜡烛烛芯内的金属可能是铜、铁、镁或铝中的一种,为确定该金属成分,请你与他继续探究并完成下列问题.(注:不考虑粉末中稀土元素对探究金属性质的影响)
(1)提出问题:蜡烛芯内的金属究竟是什么?
(2)猜想与假设:猜想一:蜡烛芯内的金属是铜;猜想二:蜡烛芯内的金属是铁;
猜想三:蜡烛芯内的金属是镁;猜想四:蜡烛芯内的金属是铝.
(3)实验验证:
a.请写出实验Ⅲ中的化学反应方程式Mg+CuSO4=MgSO4+Cu或2Al+3CuSO4=Al2(SO4)3+3Cu.
b.仅实验Ⅲ中的现象不能证明该金属一定是镁,请说明理由铝也能与硫酸铜溶液反应,也有红色固体析出.
(4)讨论交流:正确填写以下内容你将获得奖励分4分.如图是小莺利用数字实验测定的金属与酸反应时装置中压强的变化曲线.请你回答以下问题:

①图一中为什么铝条与酸反应开始一段时间压强变化不大?铝在空气中易被氧气氧化生成致密的氧化铝薄膜起到保护作用
②从图一、图二的曲线中找出一条有意义的信息:金属与酸反应时,先要打磨掉表面的氧化膜.
【查阅资料】普通蜡烛右石蜡和烛芯制成,吹不灭的蜡烛是在烛芯上包裹一层一种金属与少量稀土元素形成的合金粉末,着火点为150℃,蜡烛燃烧时,烛芯里的金属不燃烧;蜡烛一熄灭,末降温的金属就燃烧起来,从而再将蜡烛引燃.
【思考与解释】蜡烛燃烧时,烛芯里的金属为什么不燃烧?蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以燃烧.
【实验探究】小莺通过查阅资料已知吹不灭的蜡烛烛芯内的金属可能是铜、铁、镁或铝中的一种,为确定该金属成分,请你与他继续探究并完成下列问题.(注:不考虑粉末中稀土元素对探究金属性质的影响)
(1)提出问题:蜡烛芯内的金属究竟是什么?
(2)猜想与假设:猜想一:蜡烛芯内的金属是铜;猜想二:蜡烛芯内的金属是铁;
猜想三:蜡烛芯内的金属是镁;猜想四:蜡烛芯内的金属是铝.
(3)实验验证:
| 实验 | 操作步骤 | 现象 | 结论 |
| Ⅰ | 取出烛芯内的打火石,用砂纸打磨 | 金属是银白色 | 该金属一定不是铜 |
| Ⅱ | 取少量打磨后的打火石于小试管中,滴加适量稀硫酸,观察现象 | 金属逐渐溶解,有无色气体产生,溶液为无色 | 该金属一定不是铁 |
| Ⅲ | 取少量打磨后的打火石于小试管中,加入适量的氯化铜溶液,观察现象 | 有红色物质析出 | 该金属可能是镁 |
b.仅实验Ⅲ中的现象不能证明该金属一定是镁,请说明理由铝也能与硫酸铜溶液反应,也有红色固体析出.
(4)讨论交流:正确填写以下内容你将获得奖励分4分.如图是小莺利用数字实验测定的金属与酸反应时装置中压强的变化曲线.请你回答以下问题:

①图一中为什么铝条与酸反应开始一段时间压强变化不大?铝在空气中易被氧气氧化生成致密的氧化铝薄膜起到保护作用
②从图一、图二的曲线中找出一条有意义的信息:金属与酸反应时,先要打磨掉表面的氧化膜.
2.某有机物燃烧的化学方程式:X+5O2$\stackrel{点燃}{→}$3CO2+4H2O,有机物X的化学式是( )
| A. | C3H8 | B. | C3H6 | C. | C3H8O2 | D. | C3H6O |
6.肉桂酸的分子式为C9H8O2,关于肉桂酸的说法正确的是( )
| A. | 有3种元素组成 | B. | 摩尔质量为148 | ||
| C. | 氧元素的质量分数最少 | D. | 1mol分子中含有19个原子 |
16.下列实验操作正确的是( )
| A. | 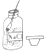 取用NaCl | B. | 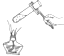 加热液体 | C. |  放置滴管 | D. | 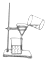 过滤 |