题目内容
3.下列说法中不正确的是( )| A. | 河水经过沉淀、过虑、活性炭吸附等净化处理后,得到的水是纯水 | |
| B. | 硬水和软水可用肥皂水区分 | |
| C. | 洗涤剂能洗涤餐具上油污的原因是洗涤剂可以使油脂乳化 | |
| D. | 实验室中含有盐酸的废水不可以直接倒入铸铁下水管道 |
分析 A、根据净化所得的水的组成分析;
B、根据硬水和软水区分方法分析;
C、洗涤剂有乳化作用;
D、根据铁与盐酸的反应分析.
解答 解:A、将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水中含有可溶质的杂质,属于混合物,不是纯水.故A说法不正确;
B、软硬水的区分可用肥皂水,硬水遇到肥皂水易起浮渣,产生的泡沫少,软水遇到肥皂水产生很多泡沫.故B说法正确;
C、洗涤剂有乳化作用,洗涤剂能洗涤餐具上油污.故C说法正确;
D、由于盐酸与铁的反应,实验室中含有盐酸的废水可以直接倒入下水道,会腐蚀下水道.故D说法正确.
故选A.
点评 本题考查的知识点较多,但难度不大,属于基础知识,应加强基础知识的学习.

练习册系列答案
相关题目
8.下列除杂方法中,所用试剂合理的是( )
| A. | 用水除去氧化钙中的碳酸钙 | |
| B. | 用氯化钡除去盐酸中混有的稀硫酸 | |
| C. | 用锌粒除去硫酸亚铁中的硫酸铜 | |
| D. | 用氢氧化钡除去碳酸钠中混有的硫酸钠 |
11.氧化镁在医药、建筑等行业应用广泛,以菱镁矿(主要成分为MgCO3,含少量FeCO3,其他杂质不溶,也不参加反应)为原料制备高纯氧化镁的实验流程如下:
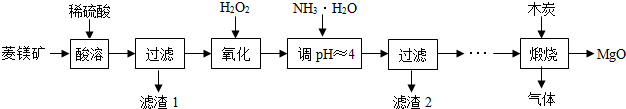
资料:①不同氢氧化物沉淀的pH范围:
②硫在常温下是一种淡黄色固体,硫的熔点约为115.2℃,沸点约为444.7℃;
③高锰酸钾溶液只吸收SO2,不吸收CO2;
④碱溶液既吸收SO2,又吸收CO2.
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为MgCO3+H2SO4=MgSO4+H2O+CO2↑.
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O.
(3)加氨水调节溶液的pH约为4的目的是,反应的化学方程式为Fe2(SO4)3+6NH3•H2O=3(NH4)2SO4+2Fe(OH)3↓,过滤后,滤液中含有种阳离子.
(4)煅烧过程存在以下反应:
2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集.(假设每步反应都完全进行)

①A中现象是:玻璃管壁出现色固体;
②B中盛放的溶液可以是d(填字母),实验现象为溶液褪色;
a.Ca(OH)2溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③C中盛放的溶液可以是氢氧化钠溶液,以吸收CO2气体,D中收集的气体是CO(填化学式).

资料:①不同氢氧化物沉淀的pH范围:
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |
③高锰酸钾溶液只吸收SO2,不吸收CO2;
④碱溶液既吸收SO2,又吸收CO2.
试回答下列问题:
(1)MgCO3与稀硫酸反应的化学方程式为MgCO3+H2SO4=MgSO4+H2O+CO2↑.
(2)加入H2O2目的是在酸性条件下将FeSO4氧化成Fe2(SO4)3,同时生成水,发生反应的化学方程式为2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O.
(3)加氨水调节溶液的pH约为4的目的是,反应的化学方程式为Fe2(SO4)3+6NH3•H2O=3(NH4)2SO4+2Fe(OH)3↓,过滤后,滤液中含有种阳离子.
(4)煅烧过程存在以下反应:
2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集.(假设每步反应都完全进行)

①A中现象是:玻璃管壁出现色固体;
②B中盛放的溶液可以是d(填字母),实验现象为溶液褪色;
a.Ca(OH)2溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③C中盛放的溶液可以是氢氧化钠溶液,以吸收CO2气体,D中收集的气体是CO(填化学式).
18.下列自然资源的利用过程中,发生了化学变化的是( )
| A. | 风力发电 | B. | 木材制桌椅 | C. | 海水晒盐 | D. | 木柴燃烧 |
8.下表是生活中一些食物的pH,有关它们的说法中不正确的是( )
| 物质种类 | 葡萄汗 | 苹果汁 | 牛奶 | 鸡蛋清 |
| pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
| A. | 苹果汁和葡萄汁都显酸性 | |
| B. | 苹果汁比葡萄汁的酸性强 | |
| C. | 鸡蛋清和牛奶都显碱性 | |
| D. | 胃酸过多的人不宜多喝葡萄汁和苹果汁 |
15. 将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
 将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )| A. | N点时,所得溶液中的溶质只有NaCl和HCl | |
| B. | M点时,所得溶液的pH>7 | |
| C. | OP段发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O | |
| D. | PM段发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ |
13.建立宏观与微观的联系是化学独特的思维方式.下列现象的微观解释中错误的是( )
| A. | 氧气加压后变成液氧,是因为氧分子分裂成了氧原子 | |
| B. | 1滴水中含有约1.67×1021个水分子,说明水分子很小 | |
| C. | 衣服在阳光下容易晒干,是因为温度越高微粒运动速率越快 | |
| D. | 非吸烟者受到被动吸烟的危害,原因之一是分子在不断地运动 |
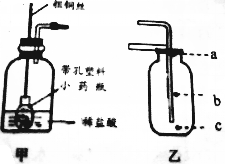 文文同学收集了一些家庭装修时废弃的大理石碎片,并查阅资料得知铜与稀硫酸、盐酸不反应,铁丝可以与稀硫酸和盐酸反应.于是他设计了如图的甲、乙两装置来制取二氧化碳,请回答下列问题:
文文同学收集了一些家庭装修时废弃的大理石碎片,并查阅资料得知铜与稀硫酸、盐酸不反应,铁丝可以与稀硫酸和盐酸反应.于是他设计了如图的甲、乙两装置来制取二氧化碳,请回答下列问题: 如图所示是被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,在其一边镀锌,可作为电池负极,另一边镀二氧化锰作为电池正极.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).
如图所示是被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,在其一边镀锌,可作为电池负极,另一边镀二氧化锰作为电池正极.电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH).