题目内容
18.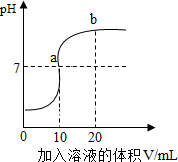 如图是测定稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( )
如图是测定稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( )| A. | 该反应是稀盐酸滴入NaOH溶液 | |
| B. | b点时,溶液的溶质为NaOH | |
| C. | a点表示反应中HCl和NaOH的质量刚好相同 | |
| D. | a点表示恰好完全反应,溶液中存在的粒子有Na+、Cl-、H2O |
分析 A、根据图象中pH值的变化是从小于7逐渐的增大到大于7,即可确定操作的过程;
B、根据该点时溶液的PH进行分析判断;
C、根据酸碱中和反应是的质量比进行分析判断;
D、B点溶液的pH大于7,溶液显碱性,所得溶液中的溶质为NaOH和NaCl,据此进行分析判断.
解答 A、由图象可知,pH值是开始时小于7逐渐的增加到等于7,然后大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH增大,说明是把氢氧化钠溶液滴加到稀盐酸中,故A错误;
B、b点时,溶液显碱性,NaOH溶液过量,此时反应已发生一段时间,溶液的溶质为NaOH、和NaCl,故B错误;
C、a点时溶液的pH等于7,反应中HCl和NaOH正好完全反应,此时二者的质量比为36.5:40,故C错误;
D、图象a点溶液的pH等于7,溶液显中性,说明二者正好完全反应,所得溶液中的溶质为H2O和NaCl,所以溶液中含有的微粒为:Na+、Cl-、H2O,故D正确.
故选D.
点评 本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
8.将空的矿泉水瓶从高原地区带到平原,瓶子变瘪,瓶内气体( )


| A. | 分子体积变小 | B. | 分子质量变小 | C. | 分子数目减少 | D. | 分子间隔变小 |
3.如图是某化学反应的微观示意图,“ ”、“
”、“ ”、“
”、“ ”分别表示不同种元素的原子,该反应可能为( )
”分别表示不同种元素的原子,该反应可能为( )

 ”、“
”、“ ”、“
”、“ ”分别表示不同种元素的原子,该反应可能为( )
”分别表示不同种元素的原子,该反应可能为( )
| A. | 水的电解 | B. | 氢气还原氧化铜 | C. | 酒精的燃烧 | D. | 甲烷的燃烧 |
17.分类是学习和研究化学物质及其变化的一种常用科学方法.下列有一组物质的分类角度与其它各组不同,该组是( )
| A. | 单质:金属单质和非金属单质 | B. | 空气:氮气、氧气和稀有气体等 | ||
| C. | 溶液:饱和溶液和不饱和溶液 | D. | 物质:纯净物和混合物 |
18.下列离子在pH=1的溶液中能大量共存,且为无色溶液的是( )
| A. | NH4+ Cl- K+ NO3- | B. | CO32- Na+ Cl- K+ | ||
| C. | Fe3+ Mg2+NO3- Cl- | D. | Na+ Ag+ NO3- Cl- |


