题目内容
8.化学研究的对象是物质,氧气、水等物质在我们的生活中非常重要.结合你对这些物质的化学知识回答下面有关问题.(1)①从微观的角度看,氧气是由氧分子构成的.氧气在化学变化中的最小粒子是氧原子,该粒子的结构示意图是C.
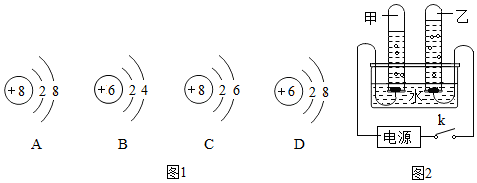
②氧气对生命和生活尤为重要,在生活中可燃物燃烧都需要氧气,写出生活中氧气与可燃物燃烧的化学反应方程式:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2(写一个)
(2)“人类依赖水,但不能创造水,只是大自然水的搬运工…”这是一句广告语.说出水的重要意义.(仅此题中①②)
①从宏观的角度看,水是由氢元素和氧元素组成的.
②人们日常生活中使用水大多数都需要对其进行净化.向水样中加入明矾搅拌溶解,因为明矾溶于水生成的胶状物可以吸附悬浮于水中的微小杂质,使水澄清.静置一段时间后,进行过滤(填操作名称),除去固体小颗粒.经过一系列净化后输送到用户的水是硬水(填“硬水”或“软水”)可加入肥皂水检验.日常生活中可采用煮沸的方法将硬水软化.
③水在通电的条件下能分解,写出该反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,在图2的装置中,当电源接通一段时间
后,甲管中气体与乙管中气体的质量比为1:8.
分析 (1)①根据物质的微粒构成解答;原子是化学变化中的最小粒子,进行分析解答即可;根据在原子中质子数=核外电子数解答;
②根据碳在氧气中充分燃烧生成二氧化碳解答;
(2)①根据物质是由元素组成的解答;
②根据已有的知识进行分析,过滤是分离不溶性固体和液体的方法,鉴别硬水和软水使用的是肥皂水,加热煮沸可以使硬水转化为软水解答;
③根据已有的知识进行分析,电解水时与正极相连的试管产生氧气,与负极相连的试管产生氢气,产生的氢气的体积是氧气体积的2倍解答.
解答 解:
(1)①氧气属于气态非金属单质,是由氧分子构成的;原子是化学变化中的最小粒子,氧气在化学变化中的最小粒子是氧原子.在原子中质子数=核外电子数=8,该粒子的结构示意图是C;
②碳在氧气中充分燃烧生成二氧化碳,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)①从宏观的角度看,水是由氢元素和氧元素组成的;
②向水样中加入明矾搅拌溶解,因为明矾溶于水生成的胶状物可以吸附悬浮于水中的微小杂质,使水澄清.要除去不溶性固体小颗粒,可以使用过滤的方法,经过一系列净化后输送到用户的水是硬水;鉴别硬水和软水使用的是肥皂水,硬水中含有较多的可溶性钙镁化合物,受热时易转化成不溶性钙镁化合物,实现硬水软化.
③水在电解时会生成氢气与氧气,方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,且正极产生氧气负极产生氢气,氧气与氢气的体积比是1:2,所以甲试管收集的气体是氢气,乙试管收集的是氧气,两者的质量比是[2×(1×2)]:(16×2)=1:8;
答案:
(1)①氧分子;氧原子;C;②C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)①氢元素和氧元素;
②吸附;过滤;硬水;肥皂水;煮沸;
③2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,1:8.
点评 本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成、分子与原子的概念是正确解答本题的关键.

| A. | 鼓励开私家车出行 | B. | 鼓励燃煤火力发电 | ||
| C. | 鼓励焚烧秸秆节约能源 | D. | 鼓励使用太阳能热水器 |
| X | Y | Z | |
| ① | H2 | O2 | CuO |
| ② | CO2 | Ca(OH)2溶液 | H2O |
| ③ | BaCl2溶液 | 稀硫酸 | K2CO3溶液 |
| ④ | Fe2O3 | CO | 稀盐酸 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③④ |
| A. | 质量比 | B. | 质量分数比 | C. | 体积比 | D. | 密度比 |
【实验一】(已知:白磷的着火点为40℃)
| 实验装置 | 实验步骤及现象 |
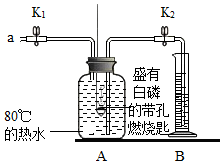 | 步骤Ⅰ.检验装置的气密性,气密性良好. 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧. 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧. 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧. |
(2)待装置冷却一段时间后,打开K2,如果观察到水倒流进A瓶40mL,说明空气中氧气的体积约占$\frac{1}{5}$.若实验测得空气中氧气的体积分数小于$\frac{1}{5}$,原因可能是气密性不好、未等装置冷却就打开夹子等(答一条即可).
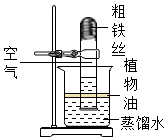
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】
| 选项 | 实验目的 | 实验方案或结论 |
| A | 除去铜粉中含有的少量铁粉 | 将混合固体加入到足量稀盐酸中,充分反应后过滤、蒸发、结晶 |
| B | 鉴别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液 | 不用其它任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③② |
| C | 除去CO2中的少量HCl气体 | 先通过过量的NaOH溶液,再通过浓硫酸 |
| D | CaCl2固体中除去CaCO3杂质 | 加水溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |