题目内容
18.通过化学学习,我们已经掌握了实验室制取气体的一般规律.如图是实验室提供的一些实验装置: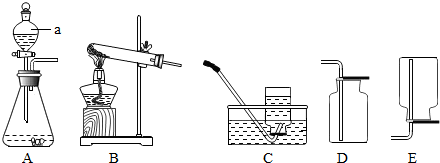
请结合图中提供的仪器回答问题.
(1)写出图中标号a的仪器名称分液漏斗,使用A装置制取气体优点控制反应速率,便于滴加药品.
(2)实验室可用高锰酸钾、双氧水来制备氧气,应选用的发生装置对应为B、A,发生反应的化学方程式分别是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,在以上选用的装置中有一种需作改进,改进的方法是试管口要有一团棉花.
(3)若用加热氯化铵和氢氧化钙的固体混合物制取氨气,则应选择的反应发生装置为B.
分析 (1)根据实验室常用仪器解答;根据装置特点分析解答;
(2)发生装置主要由反应物的状态和反应条件决定;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气;通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(3)根据发生装置主要由反应物的状态和反应条件决定解答;
解答 解:(1)根据实验室常用仪器可知:a是分液漏斗;使用A装置制取气体优点是可以控制反应速率,便于滴加液体;
(2)实验室可用高锰酸钾加热制氧气,属于固固加热型,选B;实验室用A装置制取氧气时,对反应物和反应条件的要求是:反应物是固体和液体,不需要加热,加入的试剂是过氧化氢溶液.高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;为防止高锰酸钾粉末进入导管,因此用高锰酸钾制取氧气时,试管口要有一团棉花;
(3)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;
答案:
(1)分液漏斗;控制反应速率,便于滴加药品;
(2)B、A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;试管口要有一团棉花;
(3)B.
点评 本题主要考查仪器的用途、化学方程式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

| A. | 玻璃破碎 | B. | 洗涤剂去油污 | C. | 铁丝弯曲 | D. | 光合作用 |
| 选项 | 实验目的 | 所用试剂或方法 |
| ① | 检验氯化钠中含有碳酸钠 | 加水溶解 |
| ② | 鉴别羊毛与合成纤维 | 点燃,闻气味 |
| ③ | 鉴别一氧化碳和氢气两瓶气体 | 燃着的木条 |
| ④ | 除去二氧化锰中的氯酸钾 | 加热 |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
| A. | 高能燃料燃烧 | B. | 核能发电 | C. | 大理石制成华表 | D. | 风力发电 |
| A. | 硝酸应盛放在棕色试剂瓶中 | |
| B. | 熟石灰可用于改良酸性土壤 | |
| C. | 硫酸铜可配制杀菌剂波尔多液 | |
| D. | 浓硫酸有腐蚀性,稀硫酸没有腐蚀性 |
| A. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成的有机高分子化合物 | |
| B. | 向蛋白质溶液中加入饱和硫酸钠溶液可产生黄色沉淀 | |
| C. | 由于蛋白质受热会变性,因此富含蛋白质的食物应生吃 | |
| D. | 人体内蛋白质摄入量不足,会使人生长发育迟缓、体重减轻、贫血等 |
| A. | 浓硫酸沾到皮肤上,立即用大量水冲洗 | |
| B. | 森林火灾时,砍掉一些树木形成隔离带 | |
| C. | 用点火法检查厨房内天然气是否泄漏 | |
| D. | 进入久未开启的菜窖前,用燃着的蜡烛做灯火试验 |
 碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加入碘酸钾(KIO3).如图所示为超市销售的一种加碘盐标签上的部分文字说明.
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加入碘酸钾(KIO3).如图所示为超市销售的一种加碘盐标签上的部分文字说明.