题目内容
用化学方程式解释下列现象.
(1)铝制品在空气中耐腐蚀的原因: ;
(2)铁钉浸在硝酸铜溶液中表面变成红色: ;
(3)将铝片浸入少量硫酸铜溶液中,溶液逐渐变为无色: ;
(4)铜片浸在硝酸银溶液中表面变成银白色: .
(1)铝制品在空气中耐腐蚀的原因:
(2)铁钉浸在硝酸铜溶液中表面变成红色:
(3)将铝片浸入少量硫酸铜溶液中,溶液逐渐变为无色:
(4)铜片浸在硝酸银溶液中表面变成银白色:
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,反应的化学方程式为:4Al+3O2═2Al2O3.
(2)铁钉浸在硝酸铜溶液中生成硝酸亚铁和铜,反应的化学方程式为Fe+Cu (NO3)2═Fe(NO3)2+Cu.
(3)将铝片浸入少量硫酸铜溶液中,生成硫酸铝和铜,反应的化学方程式为2Al+3CuSO4═Al2(SO4)3+3Cu.
(4)铜片浸在硝酸银溶液中生成硝酸铜和银,反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag.
故答案为:(1)4Al+3O2═2Al2O3;(2)Fe+Cu (NO3)2═Fe(NO3)2+Cu;(3)2Al+3CuSO4═Al2(SO4)3+3Cu;(4)Cu+2AgNO3═Cu(NO3)2+2Ag.
(2)铁钉浸在硝酸铜溶液中生成硝酸亚铁和铜,反应的化学方程式为Fe+Cu (NO3)2═Fe(NO3)2+Cu.
(3)将铝片浸入少量硫酸铜溶液中,生成硫酸铝和铜,反应的化学方程式为2Al+3CuSO4═Al2(SO4)3+3Cu.
(4)铜片浸在硝酸银溶液中生成硝酸铜和银,反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag.
故答案为:(1)4Al+3O2═2Al2O3;(2)Fe+Cu (NO3)2═Fe(NO3)2+Cu;(3)2Al+3CuSO4═Al2(SO4)3+3Cu;(4)Cu+2AgNO3═Cu(NO3)2+2Ag.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
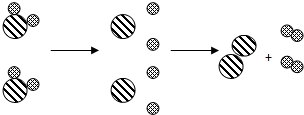 如图是水分子分解示意图.图中
如图是水分子分解示意图.图中 表示氧原子,
表示氧原子, 表示氢原子,
表示氢原子, 表示水分子,
表示水分子, 表示氧分子,
表示氧分子, 表示氢分子.从水分子分解示意图获得的信息中错误的是( )
表示氢分子.从水分子分解示意图获得的信息中错误的是( )| A、分子由原子构成 |
| B、原子是化学变化中的最小粒子 |
| C、参加化学反应的各物质在反应前后元素的种类和原子的个数都不会发生改变 |
| D、一个水分子由一个氧元素和2个氢元素构成 |
以下净水方法中能将硬水软化的是( )
| A、沉降 | B、吸附 | C、过滤 | D、蒸馏 |
下列过程属于物理变化的是( )
| A、煤的干馏 |
| B、煤和石油的形成 |
| C、秸秆、杂草等经发酵后产生甲烷 |
| D、从石油中炼制汽油、煤油等产品 |
燃烧、缓慢氧化的共同特点是( )
| A、发光 | B、放热 |
| C、需点燃 | D、发光、放热 |