题目内容
15.我国是世界钢铁产量最大的国家,赤铁矿石是炼铁的主要矿石,其主要成分为Fe2O3.计算用含Fe2O380%的赤铁矿石600t,理论上可炼出含杂质4%生铁多少吨?(杂质不含铁元素)分析 因为化学方程式中各物质都是纯净物,所以在进行含杂质的物质根据化学方程式的计算时要注意是“纯量带入”,即把不纯的物质转化为纯物质带入求算,可以据此解答.
解答 解:设3000t这种矿石,可炼出生铁质量为x,
根据题设:纯Fe2O3质量=600t×80%=4800t
纯Fe质量=x•(1-4%)=x•96%
代入化学方程式中:
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
480t x•96%
$\frac{160}{480t}=\frac{112}{x•96%}$
x=350t
答:可炼出含杂质4%的生铁350t.
点评 含杂质的物质根据化学方程式的计算,关键是要把不纯物质转化为纯物质后再带入进行求算,转化公式为:纯物质的质量=不纯物质的质量×纯度

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
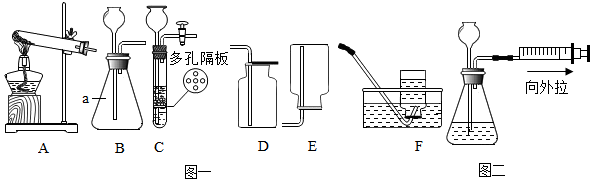
5.下列实验操作正确的是( )
| A. | 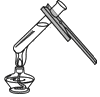 | B. |  | C. | 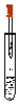 | D. | 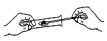 |
3.运送“天宫一号”的是“长征二号F-T1”运载火箭,火箭主要燃料是偏二甲肼(化学式为C2H8N2),下列有关偏二甲肼组成与结构的叙述,不正确的是( )
| A. | 一个偏二甲肼分子中含有一个氮气分子 | |
| B. | 由碳、氢、氮三种元素组成 | |
| C. | 是化合物 | |
| D. | 组成偏二甲肼的碳、氢、氮元素的质量比为6:2:7 |
20.空气中氧气含量测定的再认识.
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染 B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封作用 D.生成的化合物加热分解又能得到汞和氧气
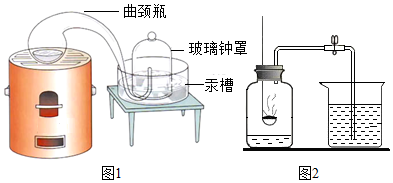
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.兴趣小组用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)红磷不足,装置内氧气有剩余;(3)…
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%.
【实验探究1】小明根据铁生锈的原理(铁能与空气中的氧气反应),探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3),通过7天测得的数据计算空气中氧气的含量为19.13%.
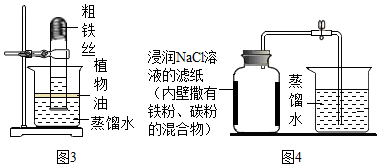
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是:装置内残留的氧气更少;实验结果更准确缺点是反应所需时间太长.
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠(NaCl)等物质又进行了实验(装置如图4),8分钟后测得的数据如表:
请计算出空气中氧气含量20.2%(计算结果保留一位小数).
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠(NaCl)进行实验,可较为快速地完成实验并减小实验误差.
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染 B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封作用 D.生成的化合物加热分解又能得到汞和氧气

【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.兴趣小组用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)红磷不足,装置内氧气有剩余;(3)…
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%.
【实验探究1】小明根据铁生锈的原理(铁能与空气中的氧气反应),探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3),通过7天测得的数据计算空气中氧气的含量为19.13%.

【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是:装置内残留的氧气更少;实验结果更准确缺点是反应所需时间太长.
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠(NaCl)等物质又进行了实验(装置如图4),8分钟后测得的数据如表:
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 130mL | 90.0mL | 63.6mL |
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠(NaCl)进行实验,可较为快速地完成实验并减小实验误差.

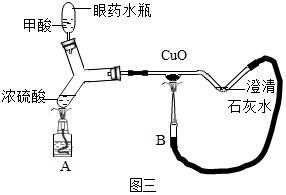
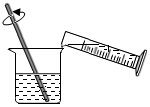 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.