题目内容
12.探究原子结构的奥秘1808年,英国科学家道尔顿提出了原子论,他认为物质都是由原子直接构成的:原子是一个实心球体,不可再分割.
1897年,英国科学家汤姆生发现原子中存在电子.他认为在原子结构中,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中.
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来.据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成.
请根据以上信息回答下列问题:
(1)科学家对原子结构的探究经历了三个过程,下列(填字母序号,下同)C是汤姆森原子结构模型,B是卢瑟福原子结构模型;
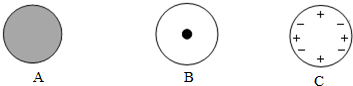
(2)在卢瑟福的实验中,大多数α粒子穿过金箔后方向不变,说明B;
A.原子的质量是均匀分布的 B.原子内部绝大部分空间是“空的”
(3)根据卢瑟福的实验所产生的现象,不能够获得的结论是D;
A.原子核体积很小 B.原子核质量较大 C.原子核带正电 D.核外电子带负电
(4)通过人类认识原子结构的历史,你对科学的发展有那些感想?(答一点即可)敢于质疑,勇于探索.
分析 根据科学家的原子模型解答,根据原子结构分析解答;原子的质量主要集中在原子核上,核外有一个非常大的空间.
解答 解:(1)据图可以看出,C是汤姆森原子结构模型,B是卢瑟福原子结构模型,故填:C,B;
(2)绝大多数α粒子穿过后方向不变,这是由于它们穿过了原子内部的空间,这也说明原子内部绝大部分空间是空的,故填:B.
(3)根据卢瑟福的实验所产生的现象,说明原子核体积很小,原子核质量较大,原子核带正电,但是不能说明核外电子带负电,故填:D;
(4)通过人类认识原子结构的历史,说明要敢于质疑,勇于探索,故填:敢于质疑,勇于探索.
点评 记住并理解原子的结构以及原子结构的发现史是解答本题关健.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
2.下列各组离子在水溶液中能大量共存的是( )
| A. | Na+、SO42-、Cl-、OH- | B. | Cu2+、Ca2+、CO32-、OH- | ||
| C. | Mg2+、NH4+、NO3-、OH- | D. | Ba2+、H+、Cl-、OH- |
20. 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )| A. | 分子总是不断运动的 | |
| B. | 分子间都是有间隔的 | |
| C. | 相同条件下,NO2气体的密度大于H2的密度 | |
| D. | 分子间有吸引力 |
7.三氟化氮(NF3)是微电子工业技术的关键原料之一,可由物质X和氟气(F2)反应得到,反应的化学方程式为:4X+3F2═NF3+3NH4F.关于物质X的下列说法不正确的是( )
| A. | 化学式为NH3 | B. | 氮元素的质量分数为25% | ||
| C. | 分子中氮、氢原子的个数比为1:3 | D. | 由氮.氢两种元素组成 |
1.请分析、比较以下几组化学反应,得出结论.
| 组别 | 化学方程式 | 结论 |
| Ⅰ | 6CO2+6H2O$\frac{\underline{\;\;\;光照\;\;\;}}{叶绿素}$C6H12O6+6O2 CO2+H2O═H2CO3 | 反应物相同,生成物不同, 原因反应条件不同. |
| Ⅱ | Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | 反应物相同,生成物不同, 原因反应物的浓度不同. |
| Ⅲ | C+O2(充足)$\frac{\underline{\;点燃\;}}{\;}$ CO2 2C+O2(不充足)$\frac{\underline{\;点燃\;}}{\;}$2CO | 反应物相同,生成物不同, 原因反应物的量不同. |
| Ⅳ | 2KClO3 $\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑(反应缓慢) 2KClO3$\frac{二氧化锰}{加热}$2KCl+3O2↑(反应迅速) | 反应物相同,反应速率不同, 原因有无催化剂. |
| 实践与应用 | 科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的“组合转化”技术,把过多二氧化碳转化为有益于人类的物质.若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: 2CO2+6H2$\frac{\underline{催化剂}}{△}$X+4H2O,推断X的化学式是C2H4. | |
17.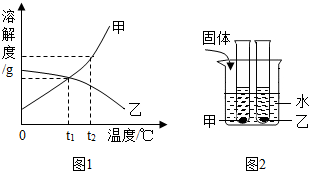 如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
 如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降到t1℃时,两种溶液中溶质质量分数相等 | |
| C. | 向烧杯的水中加氧化钙固体后,只有乙溶液中溶质的质量分数变小 | |
| D. | 甲物质中含有少量的乙物质时,可采取冷却热饱和溶液的方法获得甲物质 |