题目内容
14.同学们为证明影响物质溶解快慢的因素,设计了如下部分实验:
(1)各实验中都可观察到溶液颜色为蓝色.
(2)通过实验①②的对比,可得出的实验结论是温度越高,溶解速率越快.
(3)若要证明物质溶解的快慢与固体颗粒大小有关,需增加实验④与实验③进行对比,实验④的烧杯中需加入50mL冷水和0.5g硫酸铜粉末.
分析 根据影响固体在水中的溶解的因素进行分析解答,温度高、颗粒小,则溶解的快,依据控制变量法的具体操作进行分析.
解答 解:(1)硫酸铜在溶液中显蓝色,所以各实验中都可观察到溶液颜色为蓝色;
(2)通过对比实验①和②,可得出的实验结论是温度越高,溶解速率越快;
(3)要证明物质溶解的快慢与固体颗粒大小有关,需增加实验④与实验③进行对比,实验④的烧杯中需加入50mL冷水和0.5g硫酸铜粉末.
故答案为:(1)蓝色;
(2)温度越高,溶解速率越快;
(3)50mL冷水,0.5g硫酸铜粉末.
点评 本题考查的是影响物质溶解速率的因素,完成此题,可以依据已有的知识进行.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
4.环境保护部向媒体公布的2015年“环境日”主题是“践行绿色生活”,该主题旨在增强全民环境意识、节约意识、生态意识,选择低碳、节俭的绿色生活方式和消费模式,形成人人、事事、时时崇尚生态文明的社会新风尚,为生态文明建设奠定坚实的社会和群众基础.下面做法不符合这一主题的是( )
| A. | 推广利用太阳能、风能,缓解温室效应 | |
| B. | 工业废水处理达标后排放,防止水体污染 | |
| C. | 限制使用塑料购物袋.减少白色污染 | |
| D. | 大量使用农药化肥,提高农作物产量 |
2.在常温时有一瓶接近饱和的硝酸钾溶液,为了使其变为饱和溶液,可采取多种方法,你认为不可行的是( )
| A. | 加入硝酸钾晶体至不再溶解 | B. | 升高温度增大硝酸钾的溶解度 | ||
| C. | 降低温度至有少量晶体析出 | D. | 恒温蒸发水至有少量晶体析出 |
3.看图回答下列问题:
(1)选A、B、C、D依次组装进行实验,片刻后D装置中硫酸铜粉末由白色变为蓝色.判断:①A中产生的气体是氢气.C中的氧化铜由黑色变为红色,反应前后(用符号填充)H,Cu元素的化合价发生了变化.
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
①写出实验室制CO2的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
| A | B | C | D | E | F | |
| 装置图 | 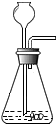 | 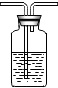 | 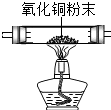 | 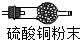 | 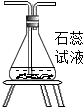 | 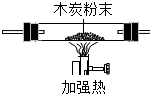 |
②B中用于干燥气体的液体是浓硫酸(填物质名称).
(2)仍选用图中装置按以下要求的顺序组装实验,在空格内填上所选的装置编号.
| 实验 要求 | 制CO2 | 证明CO2与H2O化合 | CO2→CO | CO还原性 | 除去混和气体 |
| 装置 编号 | A | E | F | C | B |
②对CO2与H2O反应后的溶液加热,可观察到石蕊试液由红色变为紫色.
③除去混合气体中的CO2,应通入(填物质的化学式)NaOH溶液.
14.除去下列物质中含有的少量杂质(括号内的物质),所选试剂不合理的是( )
| A. | CO2(CO):灼热的氧化铜 | B. | KOH溶液[Ca(OH)2]:碳酸钾溶液 | ||
| C. | CaO(CaCO3):高温煅烧 | D. | CuSO4溶液(FeSO4):铁粉 |