题目内容
16.请用所学化学知识解释下列原理.(1)用活性炭除去冰箱里的异味,是利用其吸附性.
(2)试用文字解释为什么铝制品具有良好的抗腐蚀性能:铝与空气中的氧气形成致密的氧化铝薄膜,阻止铝进一步被氧化.
(3)工业上可用Cl2与NaOH溶液作用制漂白液:Cl2+2NaOH═NaCl+NaClO+H2O.与此类似,可用Cl2与石灰乳(主要成分Ca(OH)2)制漂白粉,试写出此反应的化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
分析 (1)根据活性炭具有吸附性进行解答;
(2)根据铝制品具有良好的抗腐蚀性能是因为铝与空气中的氧气形成致密的氧化铝薄膜,阻止铝进一步被氧化进行解答;
(3)根据Cl2与石灰乳(主要成分Ca(OH)2)反应生成氯化钙、次氯酸钙和水进行解答.
解答 解:(1)活性炭具有吸附性,能除去冰箱里的异味;
(2)铝制品具有良好的抗腐蚀性能是因为:铝与空气中的氧气形成致密的氧化铝薄膜,阻止铝进一步被氧化;
(3)Cl2与石灰乳(主要成分Ca(OH)2)反应生成氯化钙、次氯酸钙和水,此反应的化学方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
故答为:(1)吸附;(2)铝与空气中的氧气形成致密的氧化铝薄膜,阻止铝进一步被氧化;(3)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评 本题考查了化学知识与在生活中的应用,完成此题,可以依据物质的性质进行.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
6.实验室需配制一定浓度的硝酸钾溶液.
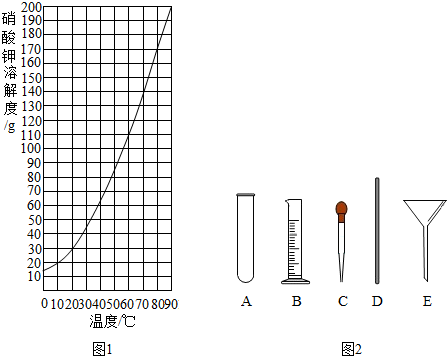
(1)查阅硝酸钾溶解性.由图可知,20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质质量分数最大为24%(计算结果保留整数).
(2)计算.配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为4g,所需蒸馏水的体积为36mL
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是图2中的BC(填字母).
(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出需要用到的数据:g/mL.
硝酸钾溶液的密度(单位g/mL)
(1)查阅硝酸钾溶解性.由图可知,20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质质量分数最大为24%(计算结果保留整数).
(2)计算.配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为4g,所需蒸馏水的体积为36mL
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是图2中的BC(填字母).

(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出需要用到的数据:g/mL.
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
7.学习了MnO2对过氧化氢分解有催化作用的知识后,小芳同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写如表:
(2)步骤①的目的是证明不加氧化铜过氧化氢能产生氧气但是速率慢.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(5)请你帮助小芳同学设计实验证明步骤⑤所得固体确实已经烘干,你的方案为:在固体上加无水硫酸铜,固体不变蓝,说明已经烘干.
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中产生气泡较快 带火星的木条复燃. | 固体质量不变 | 溶液中有气泡放出, 带火星的木条复燃 | 猜想成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(5)请你帮助小芳同学设计实验证明步骤⑤所得固体确实已经烘干,你的方案为:在固体上加无水硫酸铜,固体不变蓝,说明已经烘干.
1.下列生活中的变化属于化学变化的是( )
| A. | 用食醋除去水壶中的水垢 | |
| B. | 玻璃窗破裂 | |
| C. | 自来水通过蒸馏变成可饮用的瓶装水 | |
| D. | 用活性炭除去冰箱中的异味 |
6.下列有关说法正确的是( )
| A. | 在金属表面涂油或刷漆可以隔绝空气和水蒸气,防止金属锈蚀 | |
| B. | 催化剂在化学反应前后其化学性质发生了变化 | |
| C. | 不饱和溶液变为饱和溶液,溶质质量分数一定变大 | |
| D. | 烧碱、浓硫酸都可用来干燥氨气 |
 如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题:
如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题: