题目内容
15.等质量的Mg、Al、Zn、Fe与足量的稀硫酸反应,充分反应后产生氢气最多的是( )| A. | Mg | B. | Al | C. | Zn | D. | Fe |
分析 依据氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×参加反应的金属的质量进行分析解答.
解答 解:假设金属的质量都是1g,则
A、Mg的相对原子质量为24,则1g镁生成$\frac{1}{12}$g氢气;
B、Al的相对原子质量为27,则1g铝生成$\frac{1}{9}$g氢气;
C、Zn的相对原子质量为65,则1g铁生成$\frac{1}{32.5}$g氢气
D、Fe的相对原子质量为56,则1g铁生成$\frac{1}{28}$g氢气.
观察选项,产生氢气最多的是铝;
故选B.
点评 本题考查了有关化学方程式的计算问题,解决问题的方法有多种,解这类题的关键是明确原理找出捷径迅速解答.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
5.能保持二氧化碳化学性质的最小微粒是( )
| A. | 碳原子 | B. | 碳原子和氧原子 | C. | 氧分子 | D. | 二氧化碳分子 |
3.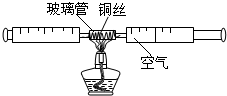 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使氧气与铜充分反应.
(2)写出该实验中硬质玻璃管里出现的现象:红色铜逐渐变成黑色,发生化学反应的文字表达式:铜+氧气$\stackrel{加热}{→}$氧化铜,反应基本类型是化合反应.
(3)小强测得实验结果如下:
由此数据可以推算出他测定的空气中氧气的体积分数小于 2l%(填“大于”或“等于”或“小于”).造成该实验出现误差的原因可能是①②③(填序号).
①交替缓缓推动两个注射器活塞次数较少;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.
 在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.
在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的硬质玻璃管加热,同时缓慢推动两个注射器活塞,过一段时间后停止加热,待冷却至室温后,将气体全部推至一支注射器内,读出注射器内气体的体积.(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是使氧气与铜充分反应.
(2)写出该实验中硬质玻璃管里出现的现象:红色铜逐渐变成黑色,发生化学反应的文字表达式:铜+氧气$\stackrel{加热}{→}$氧化铜,反应基本类型是化合反应.
(3)小强测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
①交替缓缓推动两个注射器活塞次数较少;②读数时没有冷却至室温;③加入铜丝量太少;④加入铜丝量太多.
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是通过化学反应除去混合物中的一种成分,再测量混合物在反应前后体积(或质量)的变化,从而得出该种成分的含量.
10.下列有关二氧化碳的检验、制备和用途能达到目的是( )
| A. | 二氧化碳可由木炭在足量氧气中充分燃烧产生 | |
| B. | 二氧化碳气体通入紫色石蕊试液中,溶液变为蓝色 | |
| C. | 用块状石灰石和稀硫酸迅速制备大量二氧化碳 | |
| D. | 将燃着的木条伸入集气瓶,火焰立即熄灭,证明瓶内原有气体就是二氧化碳 |

 生活中处处有化学.
生活中处处有化学.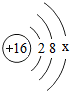 如图为某粒子结构示意图
如图为某粒子结构示意图