题目内容
13.实验室用剩的盐酸可以直接扔进下水道里吗?会产生什么样的危害?(说一条即可)怎样处理用剩的废盐酸?( 用化学方程式表示 )
分析 根据酸性废水直接排放会导致水体的污染,腐蚀铸铁管道来分析,处理废盐酸可用熟石灰进行中和.
解答 解:盐酸显酸性会腐蚀铁制管道,污染水体,所以排放前可以加碱性物质,如氢氧化钙处理成中性再排放,氢氧化钙与盐酸反应生成氯化钙和水;所以本题答案为:不可以;腐蚀下水道,污染水体,Ca(OH)2+2HCl=CaCl2+2H2O.
点评 本题考查了酸性废水的处理方法以及酸碱中和反应,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
3.下列有关溶液的说法正确的是( )
| A. | 配制好浓度为6%的NaCl溶液装瓶时不小心撒漏一部分,剩余溶液浓度仍为6% | |
| B. | 长期放置后不会分层的液体一定是溶液 | |
| C. | KNO3饱和溶液一定比不饱和溶液溶质质量分数大 | |
| D. | 降低饱和溶液的温度,一定有晶体析出 |
4.根据下面四种粒子的结构示意图判断,以下说法正确的是( )
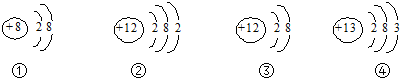
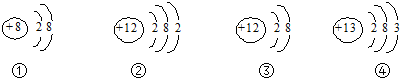
| A. | ①图是一种稀有气体元素的原子结构示意图 | |
| B. | ②图所示的粒子是一种离子 | |
| C. | ②③图所示的粒子化学性质相似 | |
| D. | ③④两图表示的是两种不同元素的微粒 |
1.实验测得人体内一些液体的PH如下,其中酸性最强的是( )
| A. | 唾液 6.6-7.1 | B. | 胃液 0.9-1.5 | C. | 汗液 6.6-7.6 | D. | 血浆 7.35-7.45 |
8.家庭饮用的纯净水,经检验其pH略小于7,这是因为水中溶有( )
| A. | NaOH | B. | CO2 | C. | NaCl | D. | O2 |
18.据报道,“第三代”瓷珠圆珠笔问世,该圆珠笔的球珠有氧化锆陶瓷材料制成,这种材料的应用使球珠的耐腐蚀性,耐磨性得到了提高,从而填补了国内空白,氧化锆的化学式为ZrO2,在氧化锆中锆元素的化合价为( )
| A. | +2 | B. | +3 | C. | +5 | D. | +4 |
5.某化学反应前后的微观示意图如图所示,下列说法正确的是( )

| A. | 该反应是置换反应 | |
| B. | 该反应有2种生成物 | |
| C. | 每个生成物分子由3个原 子构成 | |
| D. | 参加反应的“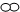 ”和“ ”和“ ”分子的个数比是 3:1 ”分子的个数比是 3:1 |

 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);