题目内容
12.“绿色化学”的特点之一是,作为原料的原子全部转化为产 品,实现“零排放”.一定条件下,CO2和H2按一定比例反应只生成1种物质,就能实现“零排放”,这种物质可能是( )| A. | 甲酸(HCOOH) | B. | 乙酸(CH3COOH) | C. | 甲醇(CH3OH) | D. | 乙醇(C2H5OH) |
分析 因为反应前是CO2和H2,H2中不含氧元素,所以生成物中的氧元素都是CO2中的,又因为化学反应前后原子个数不变,所以应从“碳与氧的原子个数为1:2”入手
解答 解:A、因甲酸的化学式为CH2O2,则一定条件下CO2和H2按1:1的比例反应就实现“零排放”,且甲酸分子中碳、氧原子个数为1:2,故A正确;
B、因乙酸的化学式为C2H4O2,分子中碳、氧原子个数不是1:2,则CO2和H2按一定比例反应不可能只生成1种物质实现“零排放”,故B错误;
C、因甲醇的化学式为CH4O,分子中碳、氧原子个数不是1:2,则CO2和H2按一定比例反应不可能只生成1种物质实现“零排放”,故C错误;
D、因乙醇的化学式为C2H6O,分子中碳、氧原子个数不是1:2,则CO2和H2按一定比例反应不可能只生成1种物质实现“零排放”,故D错误;
故选A.
点评 本题考查绿色化学,抓住物质按照一定比例在反应时只生成一种物质则可实现“零排放”是解答本题的关键,并注意反应物与生成物的构成中碳、氧的原子个数的分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.如图所示进行有关碳及其氧化物的性质实验(图中固定玻璃管的仪器已略去),下列说法正确的是( )
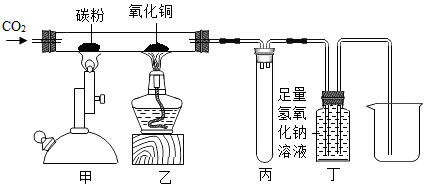

| A. | 将丁处氢氧化钠溶液改为澄清石灰水,可检验乙处反应生成的二氧化碳 | |
| B. | 乙处发生的反应属于置换反应 | |
| C. | 丙装置的作用是收集二氧化碳 | |
| D. | 甲处发生的反应中,二氧化碳作氧化剂 |
7.分析表中KNO3、NaCl两种固体的溶解度,回答下列问题:
(1)这两种物质中,溶解度受温度变化影响较大的是硝酸钾;
(2)将40gKNO3和40gNaCl分别放入100g50℃的水中,充分搅拌.
①能形成饱和溶液的物质是氯化钠;
②当降温到20℃时,析出晶体较多的是硝酸钾.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶 | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)将40gKNO3和40gNaCl分别放入100g50℃的水中,充分搅拌.
①能形成饱和溶液的物质是氯化钠;
②当降温到20℃时,析出晶体较多的是硝酸钾.
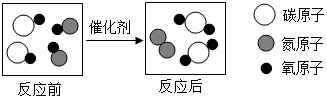 如图是某反应的围观示意图,图中的单质为N2(填化学式);反应前后化合价没有发生变化的元素为氧;生成物的质量比为22:7.
如图是某反应的围观示意图,图中的单质为N2(填化学式);反应前后化合价没有发生变化的元素为氧;生成物的质量比为22:7. 我国科学家屠呦呦因发现青蒿素(化学式为C15H22O5,一种用于治疗疟疾的药物)而获得诺贝尔奖.回答:
我国科学家屠呦呦因发现青蒿素(化学式为C15H22O5,一种用于治疗疟疾的药物)而获得诺贝尔奖.回答: