题目内容
酒精的化学式为C2H5OH,其化学名称为乙醇.下列关于乙醇的说法,正确的是
- A.乙醇是由9个原子构成的
- B.乙醇的相对分子质量为46 g
- C.乙醇中碳元素与氢元素的质量比12:1
- D.乙醇中氢元素的质量分数最小
D
分析:A、根据乙醇的微观构成进行分析判断.
B、相对分子质量单位是“1”,不是“g”,常常省略不写.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数=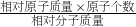 ×100%,进行分析判断.
×100%,进行分析判断.
解答:A、乙醇是由乙醇分子构成的,1个乙醇分子是由2个碳原子、6个碳原子、1个氧原子构成的,故选项说法错误.
B、相对分子质量单位是“1”,不是“g”,常常省略不写,故选项说法错误.
C、乙醇中碳元素与氢元素的质量比(12×2):(1×6)=4:1,故选项说法错误.
D、乙醇中碳原子的相对原子质量之和为12×2=24,氢原子的相对原子质量之和为1×6=6,氧原子的相对原子质量之和为16,氢元素的相对原子质量之和最大,则氢元素的质量分数最小,故选项说法正确.
故选D.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.
分析:A、根据乙醇的微观构成进行分析判断.
B、相对分子质量单位是“1”,不是“g”,常常省略不写.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数=
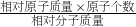 ×100%,进行分析判断.
×100%,进行分析判断.解答:A、乙醇是由乙醇分子构成的,1个乙醇分子是由2个碳原子、6个碳原子、1个氧原子构成的,故选项说法错误.
B、相对分子质量单位是“1”,不是“g”,常常省略不写,故选项说法错误.
C、乙醇中碳元素与氢元素的质量比(12×2):(1×6)=4:1,故选项说法错误.
D、乙醇中碳原子的相对原子质量之和为12×2=24,氢原子的相对原子质量之和为1×6=6,氧原子的相对原子质量之和为16,氢元素的相对原子质量之和最大,则氢元素的质量分数最小,故选项说法正确.
故选D.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
化学实验小组在整理实验药品时,实验桌上有CaCl2溶液、稀盐酸、酚酞试液和一瓶敞口的NaOH溶液.首先想到NaOH溶液已经变质了,其变质原因用化学方程式表示为______,同学们用桌上现有试剂对该瓶NaOH溶液的变质程度进行如下探究.
[提出问题]NaOH溶液是否全部变质?
[猜想]I.部分变质.
Ⅱ.全部变质.
[实验探究]
| 操作步骤 | 现象 | 结论 |
| ①取少量NaOH溶液于试管中,加入过量的______试剂 | 有白色沉淀产生 | 部分变质 |
| ②将步骤①中液体过滤,滤液中滴加酚酞试剂 | ______ |
(1)下列物质①BaCl2溶液 ②Ca(NO3)2溶液 ③Ca(OH)2溶液 ④MgCl2溶液,能替代实验操作步骤①中所用试剂的是______(填序号)
(2)NaOH溶液应如何保存______.
下列说法中正确的是
- A.铁与稀盐酸反应生成氯化铁和氢气
- B.铁片插人硫酸铜溶液中,片刻取出干燥称重,增加的质量是金属铜的质量
- C.早在西汉时期,我国劳动人民用湿法炼铜已具一定规模
- D.自来水管是镀金属锌的铁管
酸是一类重要的化合物,它能与许多物质发生化学反应,有比较广泛的用途.请你将学过的有关酸的性质与用途归纳整理,完成下面的表格.
| 酸的性质 | 发生反应的化学方程式 | 相应用途 |
| (1)酸能与多种活泼金属反应 | Zn+H2SO4=ZnSO4+H2↑ | |
| (2) | 除铁锈 |
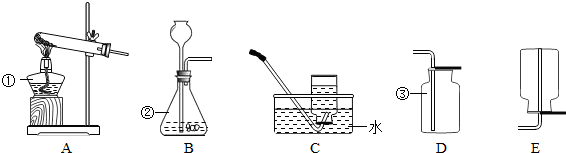
 和
和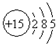 ,这两种元素的名称分别是________.当B的单质在A的单质中燃烧时,可观察到的现象是________,该反应的化学方程式为________.
,这两种元素的名称分别是________.当B的单质在A的单质中燃烧时,可观察到的现象是________,该反应的化学方程式为________.