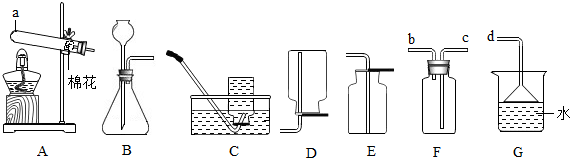
题目内容
8.不锈钢材料中含有金属铬(Cr)能提高钢的抗氧化性和耐腐蚀性.某学习小组对三种金属Cr、A1、Cu的金属活动性顺序进行探究.【提出猜想】结合所学知识,猜想三种金属的金属活动性由强到弱的关系:
猜想一:Al、Cr、Cu
猜想二:Cr、Al、Cu
猜想三:Al>Cu>Cr
【实验一】分别取三支试管,向其中加入等质量、等浓度且足量的稀硫酸,然后将用砂纸打磨过的铬、铝、铜金属片分别放入三支试管中,观察现象.
【实验现象】
| 金属 | Cr | Al | Cu |
| 与稀硫酸反应现象 | 铬片表面产生气泡较缓慢,溶液这蓝色 | 反应较剧烈,铝片表面上生气泡较快 | 无明显现象 |
【实验结论】猜想一成立.
【查阅资料】铬与稀硫酸反应生痴蓝色溶液为硫酸亚铬(CrSO4 )溶液,该反应的化学方程式为:Cr+H2SO4═CrSO4+H2↑
【实验二】取两支试管,分别向其中加入等量的CrSO4溶液,然后将用砂纸打磨过的铝、铜金属片分别放入两支试管中,观察到Al可以与CrSO4溶液反应置换出金属Cr,而Cu不与CrSO4溶液反应.
【实验小结】由上述实验得出比较金属活动性强弱的方法有两种,分别是:①金属是否与酸反应及反应的剧烈程度;②一种金属与另一种金属的化合物的溶液能否发生置换反应.
分析 【提出猜想】根据铝和铜的金属活动性铝的强,再将铬加入出现三种情况:(1)Cr、Al、Cu;(2)Al、Cr、Cu;(3)Al、Cu、Cr解答;
【实验现象】铝与稀硫酸反应生成硫酸铝和氢气;
【实验结论】根据实验现象得出正确的实验结论以及金属铬和盐酸反应生成氯化铬和氢气进行分析;
【实验小结】根据金属和酸反应产生气泡的快慢、金属和盐溶液的反应判断金属性强弱.
解答 解:【提出猜想】铝和铜的金属活动性铝的强,再将铬加入出现三种情况:(1)Cr>Al>Cu;(2)Al>Cr>Cu;(3)Al>Cu>Cr;
【实验现象】铝与稀硫酸反应生成硫酸铝和氢气,化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
【实验结论】因为铝与盐酸反应产生气泡比较激烈,而铬与稀盐酸反应产生气体比较缓慢,说明铬和铝一样排在氢的前面,但铝的活动性比铬强;铜排在氢的后面,不与盐酸反应,因此三种金属活动性的顺序为:Al>Cr>Cu,假设一成立;
【实验小结】由上述实验得出比较金属活动性强弱的方法有①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
故答案为:【提出猜想】Al、Cu、Cr;
【实验现象】2Al+3H2SO4=Al2(SO4)3+3H2↑;
【实验结论】一;
【实验小结】①金属是否与酸反应及反应的剧烈程度;②一种金属与另一种金属的化合物的溶液能否发生置换反应
点评 本题考查的是金属的活动性顺序的探究,是近几年来中考考查的重点内容之一.本题型考查实验设计的同时,也考查了学生对实验设计题的评价能力,希望同学们认真把握.

练习册系列答案
相关题目
19.我们知道氧气能使带火星的木条复燃,那么带火星的木条复燃是否一定需要纯氧呢?为了弄清这个问题,某化学探究小组进行了探究,步骤如下:
①取5个大小相同的集气瓶,分别编号1、2、3、4、5,并分别使瓶内留有占集气瓶容积10%、20%、30%、40%、
50%的水(余下为空气),用玻璃片盖住并倒扣于装有水的水槽中.
②分别用排水法向述5个瓶子中通入氧气,小心地把5个瓶子的水排完后,用玻璃片盖住瓶口,取出正放好.
③分别将带火星的木条伸入5个瓶中,观察到的现象如下:
请你参与探究,回答下列问题:
(1)从观察的现象可知,使带火星的木条复燃所需氧气的最小体积分数介于3号瓶与4号瓶之间.
(2)用排水法收集到氧气后,编号4瓶中氧气的体积分数约为52.6%.
(3)使用带火星木条检验氧气集满的方法是否可靠?否(填“是”或“否”).
(4)若要得到更准确的体积分数范围,只需调整①步骤中集气瓶内水的体积,并重复上述实验步骤即可.采取“半值法”探究能减少实验次数,你认为接下来实验应调整瓶内水占集气瓶容积的体积分数为35%.
①取5个大小相同的集气瓶,分别编号1、2、3、4、5,并分别使瓶内留有占集气瓶容积10%、20%、30%、40%、
50%的水(余下为空气),用玻璃片盖住并倒扣于装有水的水槽中.
②分别用排水法向述5个瓶子中通入氧气,小心地把5个瓶子的水排完后,用玻璃片盖住瓶口,取出正放好.
③分别将带火星的木条伸入5个瓶中,观察到的现象如下:
| 编号 | 1 | 2 | 3 | 4 | 5 |
| 现象 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
(1)从观察的现象可知,使带火星的木条复燃所需氧气的最小体积分数介于3号瓶与4号瓶之间.
(2)用排水法收集到氧气后,编号4瓶中氧气的体积分数约为52.6%.
(3)使用带火星木条检验氧气集满的方法是否可靠?否(填“是”或“否”).
(4)若要得到更准确的体积分数范围,只需调整①步骤中集气瓶内水的体积,并重复上述实验步骤即可.采取“半值法”探究能减少实验次数,你认为接下来实验应调整瓶内水占集气瓶容积的体积分数为35%.
3.将4.8g镁与足量稀H2SO4反应产生的H2,跟一定质量氯酸钾完全分解放出的O2恰好完全反应生成水,该氯酸钾的质量为( )
| A. | 4.08g | B. | 8.17g | C. | 12.26g | D. | 16.34g |
18.如表列出了1-18号元素的原子序数和元素符号:
(1)某粒子的结构示意图是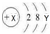 ,当X-Y=8时,该粒子的符号为S2-.
,当X-Y=8时,该粒子的符号为S2-.
(2)Cl在元素周期表中位于7(或ⅦA)主族,三周期.
(3)具有相同原子数和电子数的分子或者离子叫等电子体,等电子体具有相似的结构和性质.下列各组离子中属于等电子体的是BD
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43-和SO42-.
| 原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 元素符号 | H | He | Li | Be | B[ | C | N | O | F |
| 原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
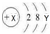 ,当X-Y=8时,该粒子的符号为S2-.
,当X-Y=8时,该粒子的符号为S2-.(2)Cl在元素周期表中位于7(或ⅦA)主族,三周期.
(3)具有相同原子数和电子数的分子或者离子叫等电子体,等电子体具有相似的结构和性质.下列各组离子中属于等电子体的是BD
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43-和SO42-.
 轻质碳酸镁 是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
轻质碳酸镁 是制取氧化镁、颜料、油漆、日用化妆品的工业原料.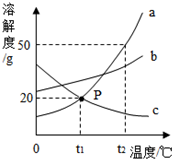 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: