题目内容
长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.为了测定水垢中碳酸钙的含量,将足量质量分数为10.0%的盐酸加 入到10.0g水垢中,产生CO2气体的情况如图所示.
(1)水垢中碳酸钙的质量分数是多少?
(2)假设水垢中除碳酸钙和氢氧化镁外,不含其它杂质,溶解10.0g水垢,至少需要质量分数为10.0%的盐酸的质量是多少?(结果保留一位小数)
(3)若配制113.0g 10.0%的稀盐酸,需用38%的浓盐酸(密度为1.19g/cm3)的体积是多少毫升?(结果精确到个位)

考点:
根据化学反应方程式的计算;有关溶质质量分数的简单计算.
专题:
综合计算(图像型、表格型、情景型计算题).
分析:
(1)根据产生CO2气体的情况图,可得知碳酸钙完全反应时放出二氧化碳3.3g;由放出二氧化碳的质量,根据碳酸钙与盐酸反应的化学方程式,计算出水垢样品中碳酸钙的质量,从而计算碳酸钙与水垢样品的质量比即水垢中碳酸钙的质量分数;
(2)分别计算水垢中碳酸钙与氢氧化镁完全反应所消耗HCl的质量,利用溶液中溶质质量分数计算公式,由溶质质量及溶液的溶质质量分数计算溶液的质量.
(3)根据溶液稀释前后溶质的质量不变分析.
解答:
解:(1)根据产生CO2气体的情况图,可得知碳酸钙完全反应时放出二氧化碳3.3g;设水垢中碳酸钙的质量为x,消耗HCl的质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 3.3g
 =
=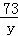 =
=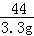
解得:x=7.5g y=5.475g
水垢中碳酸钙的质量分数=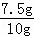 ×100%=75%
×100%=75%
答:水垢中碳酸钙的质量分数是75%;
(2)设氢氧化镁完全反应消耗HCl的质量为z
2HCl+Mg(OH)2═MgCl2+2H2O
73 58
z 10g﹣7.5g=2.5g
 =
=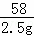
解得:z≈3.147g
至少需要质量分数为10%的盐酸的质量=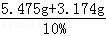 =86.2g
=86.2g
故答案为:86.2g
(3)设需用38%的浓盐酸的体积为V
113.0g×10.0%=38%×1.19g/mL×V
V=25mL
故答案为:25mL
点评:
解读折线是初中化学计算中的一种常规题型,解题时首先明确发生的化学反应,再看曲线的三点:起点、折点和终点,获得并处理信息,找到解题突破口,解答试题.设未知数按照规定不带单位.

下图1是a、b、c三种固体物质的溶解度曲线,图2表示三种固体的饱和溶液在t3℃时蒸发等量的水,析出晶体的情形。
 |
(1)图中  物质的溶解度与气体物质溶解度受温度影响变化趋势相似。
物质的溶解度与气体物质溶解度受温度影响变化趋势相似。
(2)乙烧杯中对应的溶质是 (填“a”或“b”或“c”)
(3)将 时a、b、c的饱和溶液各100 g分别升温到
时a、b、c的饱和溶液各100 g分别升温到 。若不考虑水分蒸发,下列说法正确的是 (填字母代号,下同)
。若不考虑水分蒸发,下列说法正确的是 (填字母代号,下同)
A. a、b变为不饱和溶液,c仍为饱和溶液
B. a、b两溶液溶质质量分数相等
C. a、b两溶液的质量相等
D. 溶液c中的溶 剂质量最少
剂质量最少
(4)通常情况下,在实验室用6%的a溶液配制1%的a溶液,需要到的仪器有:烧杯、 (填字母代号)。
A. 托盘天平(带砝码盒) B. 药匙 C. 玻璃棒
D. 漏斗 E. 铁架台 F. 量筒 G. 胶头滴管
下列说法正确的是( )
|
| A. | CO(NH2)2属于复合化肥 |
|
| B. | 青少年正在长身体,应多吃富含蛋白质的肉类,不吃蔬菜 |
|
| C. | 葡萄糖在人体内缓慢氧化,同时放出能量 |
|
| D. | 为了促进农作物的生长,可以大量施用化肥 |


 2AlN+3CO.若有14kg的氮气参加反应,可生成氮化铝的质量为多少?
2AlN+3CO.若有14kg的氮气参加反应,可生成氮化铝的质量为多少?