题目内容
14.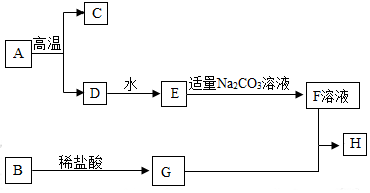 下列框图中的物质均为中学化学常见物质,其中A是大理石的主要成分,B是铁锈的主要成分,H是红褐色沉淀.下图是它们之间的转化关系,请回答.
下列框图中的物质均为中学化学常见物质,其中A是大理石的主要成分,B是铁锈的主要成分,H是红褐色沉淀.下图是它们之间的转化关系,请回答.(1)写出下列物质的化学式:CCO2,ECa(OH)2;
(2)写出B与稀盐酸反应的化学方程式:Fe2O3+6HCl=2FeCl3+3H2O;
(3)写出 F+G→H的化学方程式:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
分析 A是大理石的主要成分,B是铁锈的主要成分,H是红褐色沉淀,则A为碳酸钙,B为氧化铁,H为氢氧化铁,碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙能与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠;氧化铁与稀盐酸反应生成氯化铁和水,氯化铁与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀和氯化钠,据此进行分析解答.
解答 解:A是大理石的主要成分,B是铁锈的主要成分,H是红褐色沉淀,则A为碳酸钙,B为氧化铁,H为氢氧化铁,碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,氢氧化钙能与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠;氧化铁与稀盐酸反应生成氯化铁和水,氯化铁与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀和氯化钠,则C为二氧化碳,D为氧化钙,E为氢氧化钙,F为氢氧化钠,G为氯化铁.
(1)C、E的化学式分别是CO2、Ca(OH)2.
(2)B与稀盐酸反应,即氧化铁与稀盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.
(3)F+G→H,即氯化铁与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀和氯化钠,反应的化学方程式为:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
故答案为:(1)CO2;Ca(OH)2;(2)Fe2O3+6HCl=2FeCl3+3H2O;(3)3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
5.如表是元素周期表的一部分.这四种元素均位于第三 周期;二氧化硅与二氧化碳化学性质相似,则二氧化硅与烧碱溶液反应的化学方程式为2NaOH+SiO2═Na2SiO3+H2O.
| 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 |
2.空气成分中体积分数最大的是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | 稀有气体 |
9.绿茶中的茶多酚(化学式为C22H18O11)具有解毒和抗辐射作用.下列关于C22H18O11的说法不正确的是( )
| A. | 该物质由C、H、O三种元素组成 | |
| B. | 该物质属于化合物 | |
| C. | 该物质由22个碳原子、18个氢原子和11个氧原子构成 | |
| D. | 该物质完全燃烧能生成使澄清石灰水变浑浊的气体 |
19.下列方案合理的是( )
| A. | 验证碱能与酸反应:将H2SO4溶液滴入Cu(OH)2中 | |
| B. | 检验氧气是否集满:将带火星木条伸到集气瓶口,观察是否木条是否复燃 | |
| C. | 验证质量守恒定律:敞口试管中将锌粒与稀硫酸混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
3.下列化学用语与含义不相符的是( )
| A. | S2--硫离子 | B. | 3O-3个氧元素 | C. | Fe2O3-氧化铁 | D. | 2H2-2个氢气分子 |
4.下列有关资源、能源的叙述,不正确的是( )
| A. | 使用清洁能源、植树造林等可以更好地保护空气,防止雾霾 | |
| B. | 爱护水资源一方面要节约用水,另一方面要防止水体污染 | |
| C. | 防锈、回收、合理开采是保护金属资源的有效措施 | |
| D. | 天然气是较为清洁的可再生能源 |