题目内容
过滤的操作要点概括为:“一贴, , .”制作过滤器时,要用水湿润滤纸使其紧贴漏斗内壁的目的是 .
考点:过滤的原理、方法及其应用
专题:常见仪器及化学实验基本操作
分析:实验的设计与操作既要遵守合理性原则,又要体现安全性.具体到过滤实验,要注意“一贴、二低、三靠”三个要点.
解答:解:一贴:过滤时,为了保证过滤速度快,而且避免液体顺着漏斗与滤纸间的夹缝流下,滤纸要用水湿润滤纸使其紧贴漏斗内壁,且中间不要留有气泡.
二低:如果滤纸边缘高于漏斗边缘,过滤器内的液体极有可能溢出;如果漏斗内液面高于滤纸边缘,液体也会顺着漏斗与滤纸间的夹缝流下,这样都会导致过滤失败.
三靠:倾倒液体的烧杯口要紧靠玻璃棒,是为了使液体顺着玻璃棒缓缓流下,避免了液体飞溅;玻璃棒下端如果紧靠一层滤纸处,万一玻璃棒把湿的滤纸戳破,液体就会顺着漏斗与滤纸间的夹缝流下,导致过滤失败,而靠在三层滤纸处则能避免这一后果;漏斗下端管口的尖嘴要紧靠承接滤液的烧杯内壁,可以使滤液顺着烧杯内壁流下,避免了滤液从烧杯中溅出.
总之,“一贴、二低、三靠”,都是为了保证过滤实验操作成功.
故答案为:二低、三靠;加速过滤.
二低:如果滤纸边缘高于漏斗边缘,过滤器内的液体极有可能溢出;如果漏斗内液面高于滤纸边缘,液体也会顺着漏斗与滤纸间的夹缝流下,这样都会导致过滤失败.
三靠:倾倒液体的烧杯口要紧靠玻璃棒,是为了使液体顺着玻璃棒缓缓流下,避免了液体飞溅;玻璃棒下端如果紧靠一层滤纸处,万一玻璃棒把湿的滤纸戳破,液体就会顺着漏斗与滤纸间的夹缝流下,导致过滤失败,而靠在三层滤纸处则能避免这一后果;漏斗下端管口的尖嘴要紧靠承接滤液的烧杯内壁,可以使滤液顺着烧杯内壁流下,避免了滤液从烧杯中溅出.
总之,“一贴、二低、三靠”,都是为了保证过滤实验操作成功.
故答案为:二低、三靠;加速过滤.
点评:本题考查设计过滤实验应遵循的三个要点,既要知其然,更要知其所以然,才能一一答对.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列有关微粒的说法错误的是( )
| A、含氧元素的化合物是氧化物 |
| B、空气是由几种单质和几种化合物组成的混合物 |
| C、过氧化氢分子由氢分子和氧分子组成 |
| D、混合物的组成中肯定含有两种或两种以上的元素 |
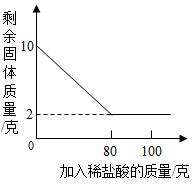 实验室常用石灰石和稀盐酸反应制取二氧化碳.某同学用质量为10克的石灰石和100克过量的稀盐酸反应,该同学测得的有关实验数据如图函数关系.(假定杂质不溶于水,也不参加反应)请回答下列问题:
实验室常用石灰石和稀盐酸反应制取二氧化碳.某同学用质量为10克的石灰石和100克过量的稀盐酸反应,该同学测得的有关实验数据如图函数关系.(假定杂质不溶于水,也不参加反应)请回答下列问题: 我们学习生物学已经知道:人体通过肺与外界进行气体交换,吸入空气中的氧气,排出的是二氧化碳和水蒸气.
我们学习生物学已经知道:人体通过肺与外界进行气体交换,吸入空气中的氧气,排出的是二氧化碳和水蒸气.