题目内容
8. (1)根据铁、铜、铝三种金属活动性顺序判断下列化学方程式正确的是③(填序号),其基本反应类型为置换反应;
(1)根据铁、铜、铝三种金属活动性顺序判断下列化学方程式正确的是③(填序号),其基本反应类型为置换反应;①3Fe+2AlCl3=3FeCl2+2Al ②3Cu+2AlCl3=3CuCl2+2Al ③Fe+CuCl2=FeCl2+Cu
(2)某实验室废液中含有HCl、ZnCl2和CuCl2等物质,若向其中加入过量的铁粉,充分反应后过滤,则滤渣中含有Fe和Cu(填化学式);
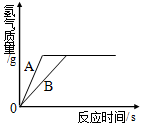
(3)用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:
①曲线A表示的是锌(填“铁”或“锌”)跟稀硫酸反应的情况.
②上述曲线图除能说明①的结论外,还可得出的结论是(答一条)稀硫酸不足.
分析 (1)在金属活动性顺序中,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来;
(2)根据金属的化学性质进行分析.
(3)根据锌、铁与酸反应的特点,判断表示反应的曲线,并分析曲线图找出反应规律.
解答 解:(1)由于铁、铜、铝的金属活动性由强到弱的顺序是铝>铁>铜,而只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,因此③Fe+CuCl2=FeCl2+Cu正确,该反应属于置换反应.故答案为:③;置换反应.
(2)由于铁可以和溶液中的HCl、CuCl2发生反应,且铁是过量的,因此充分反应后过滤,滤渣中含有生成的铜和过量的铁,故答案为:Fe和Cu.
(3)①由题中曲线,曲线A表示的金属与酸反应速度快,即金属活动性强;锌的活动性比铁强;所以曲线A表示金属锌与酸反应情况,故填:锌;
②曲线表明,等质量两种金属停止反应后产生氢气相同,这说明金属铁没有完全反应,或者说酸量不足等;
故填:稀硫酸不足.
点评 本题难度不是很大,主要考查了金属活动性顺序的应用,从而培养学生对金属活动性顺序的进一步的理解和应用.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案
相关题目
4.下列除去物质中少量杂质的方法正确的是( )
| 物质 | 杂质(少量) | 除杂方法 | |
| A | KCl | MnO2 | 加足量水溶解,过滤,洗涤,干燥 |
| B | CuO | C | 隔绝空气加热至高温 |
| C | CaO | 石灰石 | 高温煅烧 |
| D | 氧气 | 水蒸气 | 通过盛有足量浓疏酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
1.除去下列物质中少量杂质(括号内为杂质)的方法,叙述正确的是( )
| A. | 一氧化碳(二氧化碳)--通过灼热的氧化铜 | |
| B. | 水(植物油)--加洗洁精,搅拌振荡 | |
| C. | Na2CO3(NaHCO3)固体--充分加热至固体质量不变 | |
| D. | NaCl溶液(CaCl2)--滴加适量K2CO3溶液、过滤 |
3.下列选项中的实验所对应的图象错误的是( )
| A. | 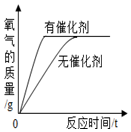 用一定量的双氧水制取氧气 | |
| B. | 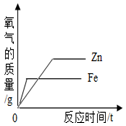 等质量Fe、Zn金属分别与足量等浓度稀硫酸反应 | |
| C. | 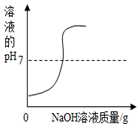 向一定量稀硫酸中逐滴加入氢氧化钠溶液 | |
| D. | 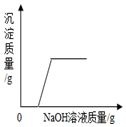 向硝酸铜和硝酸混合溶液中逐滴加入氢氧化钠溶液 |
20.下列四个图象中,能正确反映对应变化关系( )
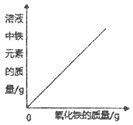 | 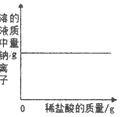 | 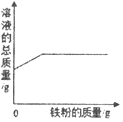 |  |
| A.向一定量的稀盐酸中加入氧化铁 | B.向一定量的氢氧化钠溶液中滴加稀盐酸 | C.向一定量的硫酸铜溶液中加入铁粉 | D.向一定量的氢氧化钠和氢氧化钙的混合溶液中通入二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
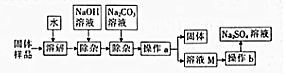
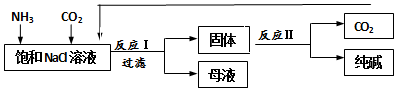
17.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展.流程简图如下,下列有关说法不正确的是( )
资料:已知铵盐均易溶于水,在受热的条件下均能分解.
资料:已知铵盐均易溶于水,在受热的条件下均能分解.

| A. | 反应中为防止氨气逸出污染空气,应先通入二氧化碳 | |
| B. | 反应I得到的另一物质在农业上可用作化肥 | |
| C. | 反应II得到的CO2循环使用可以提高物质的利用率 | |
| D. | 取过滤所得固体直接低温烘干后,加热至质量不再变化,固体质量减少6.2 g,则固体中NaHCO3的质量为16.8 g |
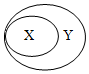 概念之间、化学反应之间具有包含、并列、交叉等关系.下表中X、Y符合如图所示关系的是( )
概念之间、化学反应之间具有包含、并列、交叉等关系.下表中X、Y符合如图所示关系的是( )