题目内容
9.摄影店中的废弃定影液中含有一定量的AgNO3,某同学为了从定影液中回收银单质.于是进行如下实验活动:(1)[回收单质银]:
①选择加入的金属:甲同学认为:向定影液中加入过量Cu粉,则得到银和铜混合物.乙同学认为:向定影液中加入过量Fe粉,则得到Fe和Ag混合物,你认为乙同学的方案更合理.其理由是便于把金属混合物分离.
②除去银粉中混有的杂质金属:向金属混合物中加入的试剂是稀盐酸,反应方程式为Fe+2HCl═FeCl2+H2↑.
(2)[进行实验]过程如下:
①废弃定影液$→_{操作a}^{加较活泼金属过量}$金属混合物+溶液A
②金属混合物$→_{操作b}^{加试剂(适量)}$Ag+溶液B
请回答:
操作a是过滤,需用到的玻璃仪器有:烧杯、玻璃棒和漏斗溶液B中溶质化学式是FeCl2.
(3)[产品验证]:请用一种简单方法验证得到的银中是否还含有铁粉,方法是磁铁吸引.
分析 (1)根据铁、铜金属的活动性分析判断;
(2)根据过滤的原理和铁与酸的反应分析回答;
(3)根据铁能被磁铁吸附、能与酸反应分析回答.
解答 解:(1)从甲和乙的实验方案可以看出虽然两种方案均可得到银,但甲方案中得到的混合物中的铜不易除去,而乙方案中得到的混合物中的铁能与盐酸或硫酸反应而被除去,反应的化学方程式是:Fe+2HCl═FeCl2+H2↑或Fe+H2SO4═FeSO4+H2↑);.
(2)由实验的过程可知,操作a能将固液分开,操作名称是过滤,过滤需用到的玻璃仪器有:烧杯、玻璃棒和漏斗;实验方案中第一步是向定影液中加入金属铁,完全反应后过滤,即可得到银和铁混合物和硝酸亚铁溶液,再向固体混合物中加入适量稀盐酸或稀硫酸,得到的溶液B即为FeCl2溶液(或FeSO4溶液).
(3)可以采用磁铁吸引的方法或与酸反应生成气体的方法.
故答案为:(1)①乙;便于把金属混合物分离.②稀HCl(或稀硫酸);Fe+2HCl═FeCl2+H2↑(或Fe+H2SO4═FeSO4+H2↑);
(2)过滤;漏斗;FeCl2(或FeSO4);
(3)磁铁吸引等.
点评 本题综合考查金属活动性顺序的应用、实验方案的设计与评价、化学方程式的书写、过滤操作等,需要多方位思考和选择.

练习册系列答案
相关题目
19.下列实验操作正确的是( )
| A. | 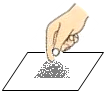 取用氯化钠 | B. |  溶解氯化钠 | C. | 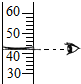 读取水的体积 | D. |  称取氯化钠 |
20.下列实验现象描述正确的是( )
| A. | 肥皂水滴入硬水中,产生较多的泡沫 | |
| B. | CO2通入无色酚酞试液,溶液变红色 | |
| C. | 红磷在氧气里剧烈燃烧,生成大量白雾 | |
| D. | NH3通入紫色石蕊试液,溶液变蓝色 |
4.分析推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 分子、原子都是不显电性的粒子,不显电性的粒子一定是分子或原子 | |
| B. | 燃烧都伴随着发光、放热现象,所以有发光、放热现象的变化就是燃烧 | |
| C. | 碱性溶液能使酚酞试液变红,能使酚酞试液变红的溶液一定是碱性溶液 | |
| D. | 盐是由金属离子和酸根离子构成的化合物,硝酸铵中没有金属离子,不属于盐 |
1.下列有关资源、能源的叙述正确的是( )
| A. | 空气是一种宝贵的资源,其中稀有气体的含量为0.03% | |
| B. | 按目前测定,海水中含有的化学物质有80多种 | |
| C. | 煤、石油、沼气、风能等都是可再生能源 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
18.如图所示实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
 (1)2003年8月以来,我国齐齐哈尔等地相继发生了侵华日军遗留的芥子气泄漏伤人事件.芥子气化学式为(C4H8Cl2S),求:芥子气的相对分子质量159,芥子气中碳、氢元素的质量比6:1.
(1)2003年8月以来,我国齐齐哈尔等地相继发生了侵华日军遗留的芥子气泄漏伤人事件.芥子气化学式为(C4H8Cl2S),求:芥子气的相对分子质量159,芥子气中碳、氢元素的质量比6:1. A~H是初中化学常见的物质,其中A为白色固体,E为黑色固体(一种金属氧化物),H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.(1)写出下列物质的化学式:ACaCO3,GCuSO4,HCu(OH)2.
A~H是初中化学常见的物质,其中A为白色固体,E为黑色固体(一种金属氧化物),H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.(1)写出下列物质的化学式:ACaCO3,GCuSO4,HCu(OH)2.