题目内容
14.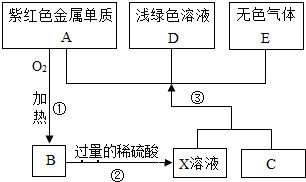 A、B、C、D、E为初中化学中常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学中常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:(1)写出A、B、C、E的化学式分别为ACu;BCuO;CFe;EH2;
(2)写出如图转化过程③中产生红色金色A的化学反应方程式Fe+CuSO4=FeSO4+Cu;
(3)写出如图转化过程③中产生无色气体E的化学反应方程式Fe+H2SO4═FeSO4+H2↑.
分析 根据题干提供的信息进行分析解答,金属单质C可以和X溶液反应生成浅绿色溶液D、紫红色金属A、无色气体E,所以可以判断D为硫酸亚铁溶液,E为氢气,而紫红色金属A为铜,所以X溶液为稀硫酸和硫酸铜铜盐溶液的混合溶液,铜能加热生成氧化铜,故B是氧化铜,可以据此结合题给的要求来完成解答即可.
解答 解:金属单质C可以和X溶液反应生成浅绿色溶液D、紫红色金属A、无色气体E,所以可以判断D为硫酸亚铁溶液,E为氢气,而紫红色金属A为铜,所以X溶液为稀硫酸和硫酸铜铜盐溶液的混合溶液,铜能加热生成氧化铜,故B是氧化铜,带入框图,推断合理;
(1)A是铜,B是氧化铜,C是铁,E是氢气,故填:Cu,CuO,Fe,H2;
(2)铁能与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4=FeSO4+Cu;
(3)铁能与硫酸反应生成硫酸亚铁和氢气,故填:Fe+H2SO4═FeSO4+H2↑.
点评 解答本题关键是要知道红色的金属单质是铜,知道浅绿色溶液是亚铁离子溶液,并要注意审题,在第②步骤中的过量稀硫酸也是解答本题的关键.

练习册系列答案
相关题目
5.下列物质的化学式,俗名完全正确的一组是( )
| A. | 纯碱NaOH | B. | 烧碱NaHCO3 | C. | 熟石灰CaO | D. | 沼气CH4 |
2.下列化学方程式书写和反应类型都正确的是( )
| A. | Cu+H2SO4═CuSO4+H2↑ 置换反应 | |
| B. | NaCl+KNO3═KCl+NaNO3 复分解反应 | |
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 | |
| D. | P+O2$\frac{\underline{\;点燃\;}}{\;}$PO2 化合反应 |
9.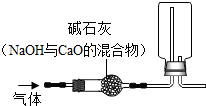 以下是我们熟悉的五种气体:
以下是我们熟悉的五种气体:
①H2 ②O2 ③CO2 ④NH3 ⑤CH4
其中可用如图所示装置干燥并收集的是(省略了铁架台等仪器)( )
 以下是我们熟悉的五种气体:
以下是我们熟悉的五种气体:①H2 ②O2 ③CO2 ④NH3 ⑤CH4
其中可用如图所示装置干燥并收集的是(省略了铁架台等仪器)( )
| A. | ①② | B. | ③④⑤ | C. | ①④⑤ | D. | ①②④⑤ |
6.下列各组物质的区分方法中,不可行的是( )
| A. | 硬水、软水--加肥皂水,搅拌观察泡沫的多少 | |
| B. | 羊毛纤维、涤纶--灼烧,闻气味 | |
| C. | 氯化钾、氯化铵--加熟石灰,研磨,闻气味 | |
| D. | 氮气、二氧化碳--用燃着的木条检验,观察燃烧的现象 |
3.向盛有10mL稀盐酸(其中滴有少量紫色石蕊溶液)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,请根据如下数据分析并回答下列问题:
(1)当加入氢氧化钠溶液的体积为10mL时,稀盐酸和氢氧化钠溶液恰好完全反应,方程式为NaOH+HCl═NaCl+H2O;
(2)当加入氢氧化钠溶液的体积为13mL时,溶液呈蓝色;
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl、HCl.
| 加入NaOH溶 液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(2)当加入氢氧化钠溶液的体积为13mL时,溶液呈蓝色;
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl、HCl.
