题目内容
5.根据如图所示装置回答问题: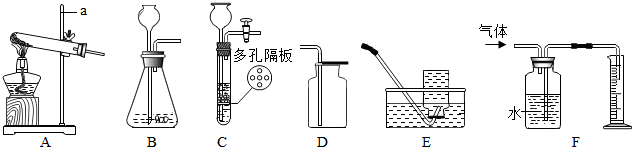
(1)图中标号仪器的名称:a铁架台.
(2)用高锰酸钾加热制取一瓶纯净的氧气应选择的装置是AE(填序号,下同),反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.实验时,判断氧气已收集满的方法是集气瓶口有气泡冒出.
(3)实验室用石灰石和稀盐酸制取二氧化碳气体,若要随时使反应发生或停止,应选用的发生装置是C,该装置能否用于过氧化氢溶液和二氧化锰粉末混合制氧气?不能(选填“能”或“不能”)
(4)小伟将B和F装置连接,加入药品充分反应后,通过排出水的量测定生成气体的体积.实验结束时,发现实际测定的数值大于理论值(气体难溶于水,实验测定的数据无误),其主要原因是该反应是放热反应.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,排水法收集的氧气纯净,排空气法收集的氧气干燥,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据多孔隔板可以通过液体的压强将固体和液体隔离,二氧化锰是粉末状,多孔隔板不能将固体和液体分离进行分析;
(4)根据气体难溶于水,实验测定的数据无误,实验结束时,发现实际测定的数值大于理论值,原因可能是:反应是放热反应,导致气体膨胀进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是铁架台;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,排水法收集的氧气纯净,排空气法收集的氧气干燥,所以用高锰酸钾加热制取一瓶纯净的氧气应选择的装置是AE,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验时,判断氧气已收集满的方法是:集气瓶口有气泡冒出;
(3)多孔隔板可以通过液体的压强将固体和液体隔离,所以应选用的发生装置是:C,二氧化锰是粉末状,多孔隔板不能将固体和液体分离,所以该装置不能用于过氧化氢溶液和二氧化锰粉末混合制氧气;
(4)气体难溶于水,实验测定的数据无误,实验结束时,发现实际测定的数值大于理论值,原因可能是:反应是放热反应,导致气体膨胀.
故答案为:(1)铁架台;
(2)AE,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,集气瓶口有气泡冒出;
(3)C,不能;
(4)该反应是放热反应.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案| A. |  苹果 | B. |  菠萝 | C. |  柿子 | D. |  番茄 |
| A. | 面粉 | B. | 食盐 | C. | 食用油 | D. | 奶粉 |
| A. | 亚硝酸中钠、氧元素的质量比为23:32 | |
| B. | 亚硝酸钠中氧元素的质量分数最小 | |
| C. | 亚硝酸钠是氧化物 | |
| D. | 亚硝酸钠中氮元素化合价为+5价 |

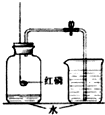 某实验小组用图所示装置来测定空气中氧气的含量.
某实验小组用图所示装置来测定空气中氧气的含量.