题目内容
1.实验室中,利用下列装置可以制取某些气体,请回答下列问题.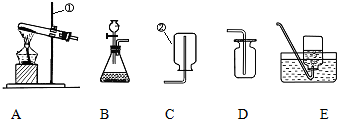
(1)写出带标号的仪器的名称:①铁架台;②集气瓶.
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性.
(3)实验室若用高锰酸钾制取氧气,选择的发生装置是A,收集装置是D或 E.其化学反应方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(4)如果用排水法集气时,当观察气泡均匀连续 放出时就可以收集.当停止反应时,如果先熄灭酒精灯,再把导管从水槽里撤出,造成的后果是水槽中的水会沿着导管倒流进入试管,使试管骤冷而炸裂.证明一瓶无色气体是氧气的方法是:用带火星的木条放在无色气体瓶口,若木条复燃.证明这瓶无色气体是氧气.
(5)用双氧水制氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
选择的发生装置是B.该装置的优点是:可控制反应的速率.
(6)用向上排空气法收集氧气时,欲检验集气瓶里氧气是否已收集满,采用的方法是将带火星的木条平放在集气瓶口,若木条复燃证明氧气已满,反之则不满.
分析 (1)根据常见仪器的名称和用途分析;
(2)根据制取气体前要先检查装置的气密性再装药品分析;
(3)根据高锰酸钾是固体需加热所以选择固体加热型制取装置,氧气的密度比空气大可用向上排空气法收集,氧气的不易溶于水所以可选用排水法收集,高锰酸钾加热生成锰酸钾、二氧化锰和氧气分析;
(4)根据实验室制取氧气的气体收集和注意问题,并利用氧气的助燃性来检验分析..
(5)用过氧化氢制取氧气,属于固液常温型,故选发生装置B,双氧水在二氧化锰作催化剂的条件下生成水和氧气并据此反应原理书写方程式;
(6)根据氧气的性质分析,检验集气瓶中氧气是否收集满要用带火星的木条,且要平放在集气瓶口.
解答 解:(1)铁架台用于固定,集气瓶用于收集气体;故答案:①铁架台②集气瓶;
(2)制取气体前要先检查装置的气密性再装药品;故答案:检查装置的气密性;
(3)高锰酸钾是固体需加热所以选择固体加热型制取装置,氧气的密度比空气大可用向上排空气法收集,氧气的不易溶于水所以可选用排水法收集;高锰酸钾加热生成锰酸钾、二氧化锰和氧气;故答案:A; D E; 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)如果用排水法集气时,当气泡均匀连续的冒出时,再收集气体,会比较纯净;因用排水法集气时,开始装置中的空气还没有排净,当气泡均匀连续冒出时,得到的才是纯净的氧气;当停止反应时,如果先熄灭酒精灯,试管中气体减少,在外压作用下,水槽中的水会沿着导管倒流进入试管,使试管骤冷而炸裂;根据氧气的助燃性,可使用带火星的木条放在无色气体瓶口,若木条复燃.证明这瓶无色气体是氧气.故答案为:气泡均匀连续的冒出;水槽中的水会沿着导管倒流进入试管,使试管骤冷而炸裂;用带火星的木条放在无色气体瓶口,若木条复燃.证明这瓶无色气体是氧气;
(5)双氧水在二氧化锰作催化剂的条件下生成水和氧气,所以方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;用过氧化氢制取氧气,属于固液常温型,故选发生装置B,该装置的优点是:可控制反应的速率;故答案:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;可控制反应的速率;
(6)氧气能使带火星的木条复燃,检验集气瓶中氧气是否收集满要用带火星的木条,且要平放在集气瓶口,因此验满的方法是将带火星的木条平放在集气瓶口,若木条复燃证明氧气已满,反之则不满.
故答案:将带火星的木条平放在集气瓶口,若木条复燃证明氧气已满,反之则不满.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强;气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

| 选项 | 物质(括号内为杂质) | 选用试剂 | 操作方法 |
| A | Fe(Cu) | 足量的盐酸 | 过滤、蒸发、结晶 |
| B | CuSO4(Fe) | 水 | 过滤、蒸发 |
| C | CO2(CO) | O2 | 点燃 |
| D | ZnCl2(CuCl2) | 过量的Zn粉 | 加水溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 光合作用 | B. | 粮食酿酒 | C. | 火药爆炸 | D. | 湿衣服晾干 |
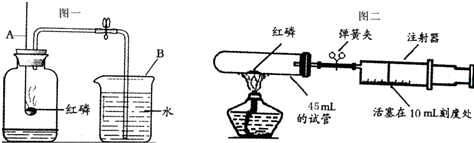
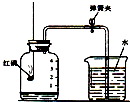 空气是人类赖以生存的自然资源.测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.
空气是人类赖以生存的自然资源.测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.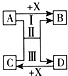 A、B、C、D、X为初中常见的五种物质,请根据要求回答问题.
A、B、C、D、X为初中常见的五种物质,请根据要求回答问题.