题目内容
12.下列各组离子中,能大量共存的是( )| A. | H+、SO42-、OH-、Ba2+ | B. | Na+、K+、Cl-、SO42- | ||
| C. | Na+、H+、NO3-、CO32- | D. | K+、Mg2+、NO3-、OH- |
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可.
解答 解:A、SO42-、Ba2+结合生成硫酸钡沉淀,H+、OH-结合生成水,不能大量共存,故选项错误.
B、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确.
C、H+、CO32-结合生成水和二氧化碳,不能大量共存,故选项错误.
D、Mg2+和OH-结合生成氢氧化镁沉淀,不能大量共存,故选项错误.
故选:B.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
2.下列实验操作错误的是( )
| A. | 用胶头滴管吸取并滴加试剂后,立即用蒸馏水冲洗干净 | |
| B. | 加热试管里的药品时,要先预热试管 | |
| C. | 将块状固体放入直立的试管内 | |
| D. | 用药匙取固体药品后,立即用干净的纸擦拭干净 |
20.下列说法正确的是( )
| A. | 80gNH4NO3与60g尿素CO(NH2)2肥效相同 | |
| B. | 84gNaHCO3和MgCO3以任意比例混合后与足量盐酸反应,一定产生44gCO2 | |
| C. | 镁和金属X的混合物共2.4g加入足量的稀硫酸,充分反应后得到0.22gH2,则金属X可能是Zn | |
| D. | 等质量、等质量分数的氢氧化钠溶液与稀硫酸充分反应后,所得溶液显中性 |
7.下列化肥中,从外观即可与其他化肥相区别的是( )
| A. | 磷矿粉 | B. | 尿素 | C. | 硫酸钾 | D. | 硝酸铵 |
17.“金、银、铜、铁、锡”俗称五金.这五种金属中,金属活动性最强的是( )
| A. | 铁 | B. | 金 | C. | 锡 | D. | 铜 |
4.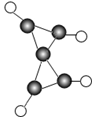 科学家在-100℃合成了化合物X(分子模型如图,其中
科学家在-100℃合成了化合物X(分子模型如图,其中 代表碳原子,
代表碳原子, 代表氢原子).下列说法正确的是( )
代表氢原子).下列说法正确的是( )
 科学家在-100℃合成了化合物X(分子模型如图,其中
科学家在-100℃合成了化合物X(分子模型如图,其中 代表碳原子,
代表碳原子, 代表氢原子).下列说法正确的是( )
代表氢原子).下列说法正确的是( )| A. | X是有机高分子化合物 | |
| B. | X中碳元素的质量分数为93.75% | |
| C. | X中氢原子与碳原子的个数比为5:4 | |
| D. | 等质量的X与甲烷完全燃烧,X消耗的氧气多 |
1.下列属于纯净物的是( )
| A. | 冰红茶 | B. | 液态氮 | C. | 碳素钢 | D. | 大理石 |
2.实验室有一瓶敞口久置的烧碱药品,取20g此样品加水溶解配制成120g溶液,加入氯化钙溶液至恰好完全反应,实验过程如下(不考虑氯化钙与氢氧化钠反应),下列说法正确的是( )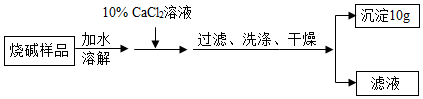

| A. | 滤液中溶质只有氯化钠 | |
| B. | 加入氯化钙溶液的质量为111g | |
| C. | 用氯化钡替代氯化钙所得沉淀质量变大,相对误差偏大 | |
| D. | 样品中氢氧化钠的质量小于9.4g |
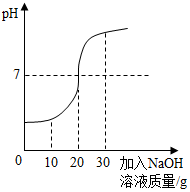 化学兴趣小组对某工业废水(溶质为HCl、NaCl)中的HCl含量进行测定,甲、乙两位同学各提供不同的测定方法:
化学兴趣小组对某工业废水(溶质为HCl、NaCl)中的HCl含量进行测定,甲、乙两位同学各提供不同的测定方法: