题目内容
2.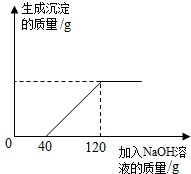 现有含HCl和CuCl2的混合溶液100g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成Cu(OH)2沉淀的质量与加入NaOH溶液的质量关系如图所示.
现有含HCl和CuCl2的混合溶液100g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成Cu(OH)2沉淀的质量与加入NaOH溶液的质量关系如图所示.(1)加入40gNaOH溶液前无沉淀生成的原因是因为NaOH溶液先与盐酸反应无沉淀生成.
(2)求原混合溶液中CuCl2的质量分数.
分析 (1)根据酸与碱发生中和反应分析回答;
(2)根据氢氧化钠与氯化铜反应的哈学方程,由与氯化铜反应氢氧化钠质量可求出混合溶液中CuCl2的质量,再根据溶液的溶质的质量分数计算.
解答 解:(1)因为NaOH溶液先与盐酸反应无沉淀生成;
(2)设混合溶液中CuCl2的质量为x.
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 80
x (120-40)×10%g
$\frac{135}{80}=\frac{x}{(120g-40g)×10%}$ x=13.5g
混合溶液中CuCl2的质量分数=$\frac{13.5g}{100g}×100%$=13.5%
答:(1)加入40gNaOH溶液前无沉淀生成的原因是NaOH溶液先与盐酸反应无沉淀生成.
(2)求原混合溶液中CuCl2的质量分数是13.5%.
点评 本题主要考查学生利用化学方程式和溶质质量分数公式进行计算的能力,学生要有较强的识图能力和数据分析能力,才能正确解答.

练习册系列答案
相关题目
17.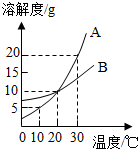 如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )
如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )
 如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )
如图是A、B两种固体物质的溶解度曲线,下列说法错误的是( )| A. | 20℃时,A、B两种物质的溶解度相等 | |
| B. | 30℃时,A的饱和溶液中溶质质量分数大于B的饱和溶液中溶质质量分数 | |
| C. | B物质的饱和溶液从30℃降温到10℃,变成不饱和溶液 | |
| D. | 若A中含有少量的B,可用冷却热饱和溶液的方法提纯A |
7.在一密闭容器内,充入a个一氧化碳分子和b个氧分子,在一定条件下,使其恰好完全反应,反应后容器中碳原子数和氧原子数之比为( )
| A. | a:(a+2b) | B. | a:2(a+b) | C. | a:b | D. | a:2b |
14.氯气(Cl2)是黄绿色气体,氯气的水溶液叫氯水,把品红试纸(浸染有品红的试纸)伸入氯水中,品红褪色.
【提出问题】氯水中的哪些成分能使品红褪色呢?
【查阅资料】氯气溶于水,部分与水反应,方程式为Cl2+H2O═HCl+HClO.其中,HClO的名称,叫次氯酸,是一种弱酸,具有强氧化性.
【猜 想】猜想1:是氯水中的水使品红褪色的.
猜想2:是氯水中的Cl2(填化学式)使品红褪色的.
猜想3:是氯水中的盐酸使品红褪色的.
猜想4:是氯水中的次氯酸使品红褪色的.
【实验探究】
【结 论】综合分析可得:氯水中的HClO(填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色).
【反 思】(1)HClO中,氯元素的化合价为+1价.
(2)向氯水中滴加紫色石蕊试液,观察到的现象是先变红,后褪色.
【提出问题】氯水中的哪些成分能使品红褪色呢?
【查阅资料】氯气溶于水,部分与水反应,方程式为Cl2+H2O═HCl+HClO.其中,HClO的名称,叫次氯酸,是一种弱酸,具有强氧化性.
【猜 想】猜想1:是氯水中的水使品红褪色的.
猜想2:是氯水中的Cl2(填化学式)使品红褪色的.
猜想3:是氯水中的盐酸使品红褪色的.
猜想4:是氯水中的次氯酸使品红褪色的.
【实验探究】
| 实验操作 | 实验现象 | 过程分析 |
| ①把品红试纸深入水中 | 没有褪色 | 猜想1不成立 |
| ②把品红试纸渗入干燥的氯气中 | 没有褪色 | 猜想2不成立 |
| ③把品红试纸伸入盐酸中 | 没有褪色 | 猜想3不成立 |
【反 思】(1)HClO中,氯元素的化合价为+1价.
(2)向氯水中滴加紫色石蕊试液,观察到的现象是先变红,后褪色.
11.受蒙古气旋和冷空气影响,2010年3月19日,我国出现了今年以来最强的一次沙尘暴天气.以下关于( )
| A. | 沙尘漂浮在空气中是由于分子运动造成的 | |
| B. | 为了防止沙尘暴的发生,应保护草原植被 | |
| C. | 出现沙尘暴时,外出要戴好口罩,以免沙尘伤害呼吸道 | |
| D. | 沙尘掉落在叶片上会使植物的光合作用减弱 |
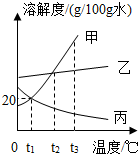 如图所示是甲、乙、丙三种固体物质的溶解度曲线.
如图所示是甲、乙、丙三种固体物质的溶解度曲线.