题目内容
将一定质量的氯化钠和碳酸钠的混合物加水溶解,再向此溶液中加入50g一定溶质质量分数的稀盐酸,恰好完全反应.经数据分析可知放出气体4.4g,经测定,滤液中含氯元素的质量21.3g(假定物质质量无损失).求:
(1)所加稀盐酸的溶质质量分数.
(2)原固体混合物中氯化钠的质量.
(1)所加稀盐酸的溶质质量分数.
(2)原固体混合物中氯化钠的质量.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据碳酸钠与盐酸反应的方程式,由生成的二氧化碳的质量可求出碳酸钠的质量、盐酸中溶质的质量,根据溶质质量分数的计算公式,求出稀盐酸的溶质质量分数;根据化学式的意义、根据滤液中含氯元素的质量求出总的氯化钠的质量,减去生成的氯化钠质量就是原固体混合物中氯化钠的质量.
解答:解:(1)设所加稀盐酸中HCl的质量为x,生成的NaCl的质量为y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
73 117 44
x y 4.4g
=
=
解得:x=7.3g y=11.7g
所加稀盐酸的溶质质量分数:
×100%=14.6%
(2)设滤液中溶质的质量为z
2NaCl~2Cl
117 71
z 21.3g
=
解得:z=35.1g
原固体混合物中氯化钠的质量为:35.1g-11.7g=23.4g
答:(1)所加稀盐酸的溶质质量分数是14.6%.(2)原固体混合物中氯化钠的质量是23.4g.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
73 117 44
x y 4.4g
| 73 |
| x |
| 117 |
| y |
| 44 |
| 4.4g |
解得:x=7.3g y=11.7g
所加稀盐酸的溶质质量分数:
| 7.3g |
| 50g |
(2)设滤液中溶质的质量为z
2NaCl~2Cl
117 71
z 21.3g
| 117 |
| 71 |
| z |
| 21.3g |
原固体混合物中氯化钠的质量为:35.1g-11.7g=23.4g
答:(1)所加稀盐酸的溶质质量分数是14.6%.(2)原固体混合物中氯化钠的质量是23.4g.
点评:根据方程式中物质的质量比,有一种物质的质量可以计算另一种物质的质量,解题时要根据题意细心分析解答.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
要配制质量分数为20%的硫酸溶液,需用质量分数分别为60%、10%的硫酸溶液的质量比为( )
| A、1:3 | B、1:5 |
| C、1:6 | D、1:4 |
下列四种变化中,与其他三种变化有本质区别的是( )
| A、生石灰放置在潮湿的空气中,质量增加 |
| B、浓盐酸敞放置在空气中,质量减少 |
| C、氢氧化钠固体暴露在空气中,质量增加 |
| D、化肥碳铵敞放在空气中,质量减少 |
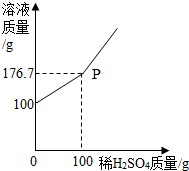 为测定某BaCl2溶液的溶质质量分数,现取100g BaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,请回答:
为测定某BaCl2溶液的溶质质量分数,现取100g BaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,请回答: