题目内容
根据二氧化碳的化学式(CO2)计算.
(1)求物质的相对分子质量
(2)二氧化碳里碳元素和氧元素的质量比;
(3)二氧化碳里碳元素的质量分数;
(4)11g二氧化碳含碳多少克.
(1)求物质的相对分子质量
(2)二氧化碳里碳元素和氧元素的质量比;
(3)二氧化碳里碳元素的质量分数;
(4)11g二氧化碳含碳多少克.
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数公式进行分析解答.
(4)根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数公式进行分析解答.
(4)根据元素的质量=化合物的质量×化合物中该元素的质量分数来分析解答.
解答:解:(1)二氧化碳的相对分子质量为12+16×2=44.故填:44;
(2)二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8.故填:3:8;
(3)二氧化碳含有碳元素的质量分数是:
×100%≈27.3%.故填:27.3%;
(4)11克里二氧化碳含有碳元素的质量为11g×
×100%=4g.故填:4g.
(2)二氧化碳里碳元素和氧元素的质量比是12:(16×2)=3:8.故填:3:8;
(3)二氧化碳含有碳元素的质量分数是:
| 12 |
| 12+16×2 |
(4)11克里二氧化碳含有碳元素的质量为11g×
| 12 |
| 44 |
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
按下述实验方法制备气体,合理的是( )
| A、用酒精灯加热碳酸钙制二氧化碳 |
| B、大理石与稀硫酸反应制二氧化碳 |
| C、木炭和氧气反应二氧化碳 |
| D、双氧水和二氧化锰的混合物制氧气 |
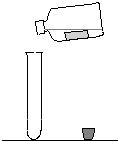 在练习取用液体时,小郑用如图所示的操作来进行,请你至少指出他的三种错误:
在练习取用液体时,小郑用如图所示的操作来进行,请你至少指出他的三种错误: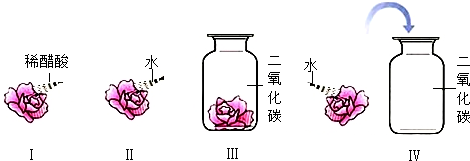
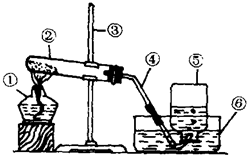 如图是用氯酸钾和二氧化锰制取氧气的实验装置,请回答:
如图是用氯酸钾和二氧化锰制取氧气的实验装置,请回答:
 (1)天然气燃烧时产生的热量高且产物都是无毒物质,是一种理想的燃料.天然气的主要成分是(填化学式)
(1)天然气燃烧时产生的热量高且产物都是无毒物质,是一种理想的燃料.天然气的主要成分是(填化学式) 据图回答:
据图回答: