题目内容
将质量相等的烧杯放在天平两端,加入等质量、等质量分数的盐酸,向左端烧杯中加入2.7g铝,向右端烧杯加2.7g镁,则反应停止时,天平指针将可能指向( )
| A、中间 | B、左端 |
| C、右端 | D、三种情况都有可能 |
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:本题考查了金属与酸的反应,由题目的信息可知:将质量相等的烧杯放在天平两端,加入等质量、等质量分数的盐酸,在左、右盘的烧杯中分别加入质量相等的铝和镁,反应停止后,观察天平是否保持平衡.两种情况:两种金属都过量,则放出的氢气一样多,因此盐酸一定完全反应,天平保持平衡;如果酸过量,则生成的氢气=
×金属质量,则可知左端烧杯生成氢气多,则偏轻.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:
由题目的信息可知:将质量相等的烧杯放在天平两端,加入等质量、等质量分数的盐酸,在左、右盘的烧杯中分别加入质量相等的铝和镁,反应停止后,观察天平是否保持平衡.两种情况:两种金属都过量,则放出的氢气一样多,因此盐酸一定完全反应,天平保持平衡;如果酸过量,则生成的氢气=
×金属质量,则可知左端烧杯生成氢气多,则偏轻.
故选:AC.
由题目的信息可知:将质量相等的烧杯放在天平两端,加入等质量、等质量分数的盐酸,在左、右盘的烧杯中分别加入质量相等的铝和镁,反应停止后,观察天平是否保持平衡.两种情况:两种金属都过量,则放出的氢气一样多,因此盐酸一定完全反应,天平保持平衡;如果酸过量,则生成的氢气=
| 金属的化合价 |
| 金属的相对原子质量 |
故选:AC.
点评:本考点考查了酸的性质,金属与酸反应生成盐和氢气,有关的计算要准确,本考点主要出现在选择题和实验题中.

练习册系列答案
相关题目
下列化学方程式的书写错误的是( )
A、Mg+O2
| ||||
B、4P+5O2
| ||||
| C、Fe+CuSO4=FeSO4+Cu | ||||
D、C+O2
|
下列关于分子、原子、离子的说法中,正确的是( )
| A、在化学反应中,分子能再分,原子不能再分 |
| B、原子都是由质子、中子、电子构成的 |
| C、分子、原子、离子都能构成物质 |
| D、分子、原子都能保持所构成物质的化学性质 |
下列化学方程式不符合客观事实在是( )
| A、石灰浆抹墙后,久之变硬 Ca(OH)2+CO2=CaCO3↓+H2O | ||||
| B、不能用铁桶盛装波尔多液的原因是 Fe+CuSO4=FeSO4+Cu | ||||
C、炼铁高炉中发生的主要反应 Fe2O3+3CO
| ||||
| D、不用指示剂,恰好除去氯化钙溶液中的盐酸 CaO+2HCl=CaCl2+H2O |
生活中下列现象属于化学变化的是( )
| A、冰雪融化 | B、气球吹大了爆炸 |
| C、玻璃破碎 | D、煤燃烧 |
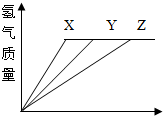 将质量相等的镁、锌、铁三种金属,同时分别放入三份质量分数相同且等质量的稀盐酸中,反应生成的氢气与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是( )
将质量相等的镁、锌、铁三种金属,同时分别放入三份质量分数相同且等质量的稀盐酸中,反应生成的氢气与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是( )| A、图线X表示镁的反应情况 |
| B、盐酸都已完全反应 |
| C、镁、锌一定过量,铁可能反应完 |
| D、锌可能反应完,镁、铁一定过量 |
下列物质中,常温下易溶于水的是( )
| A、氧气 | B、面粉 | C、蔗糖 | D、植物油 |