题目内容
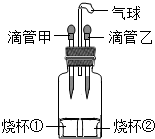 (2012?平顶山二模)如图装置可以完成多个实验,具有药品用量少、现象明显、尾气不外逸等优点.
(2012?平顶山二模)如图装置可以完成多个实验,具有药品用量少、现象明显、尾气不外逸等优点.(1)若滴管甲中吸有浓氨水,滴管乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞溶液变红,主要说明分子具有的什么性质.
分子是不断运动的
分子是不断运动的
.(2)若滴管甲中吸有水,滴管乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末.依次将甲、乙中的液体滴入烧杯①、②中,可观察的现象是什么?
烧杯②中有大量气体逸出;烧杯①中的纸花由紫色变为红色
烧杯②中有大量气体逸出;烧杯①中的纸花由紫色变为红色
.(3)若滴管甲中的液体是水,且挤出后观察出气球明显鼓起,一段时间后恢复原状,则烧杯中的固体可能是什么物质?
可能是氢氧化钠(或生石灰等)
可能是氢氧化钠(或生石灰等)
;若该现象是由发生化合反应而引起的,则该反应的化学方程式是CaO+H2O=Ca(OH)2
CaO+H2O=Ca(OH)2
.分析:(1)根据分子的基本性质分析;
(2)根据碳酸盐与酸反应生成二氧化碳气体,二氧化碳气体溶于水生成碳酸分析;
(3)根据气球膨胀可能由于产生气体或溶于水放热来考虑.
(2)根据碳酸盐与酸反应生成二氧化碳气体,二氧化碳气体溶于水生成碳酸分析;
(3)根据气球膨胀可能由于产生气体或溶于水放热来考虑.
解答:解:(1)由于氨水和酚酞试液不在一个烧杯中,但酚酞试液变红了,说明氨水进入了酚酞试液中,氨水显碱性能使酚酞试液变红,所以说明了氨分子在不断运动,才运动到酚酞试液中的,所以说明分子在不断运动;
(2)通过硫酸与碳酸钠反应产生二氧化碳,会看到烧杯②中有大量气体生成,生成的二氧化碳溶于水生成碳酸,碳酸能使紫色石蕊试液变红色;
(3)由于甲中滴管是水,所以该物质溶于水放出热量,溶于水放热的有浓硫酸、氢氧化钠固体、生石灰,浓硫酸是液体,不合题意,所以烧杯①中可以氢氧化钠固体、生石灰;若该现象是由发生化合反应而引起的,那么就是氧化钙和水反应生成了氢氧化钙,则该反应的化学方程式是 CaO+H2O=Ca(OH)2
故答案为:(1)分子是不断运动的 (2)烧杯 ②中有大量气体逸出,烧杯①中的纸花由紫色变为红色;
(3)可能是氢氧化钠(或生石灰等),CaO+H2O=Ca(OH)2
(2)通过硫酸与碳酸钠反应产生二氧化碳,会看到烧杯②中有大量气体生成,生成的二氧化碳溶于水生成碳酸,碳酸能使紫色石蕊试液变红色;
(3)由于甲中滴管是水,所以该物质溶于水放出热量,溶于水放热的有浓硫酸、氢氧化钠固体、生石灰,浓硫酸是液体,不合题意,所以烧杯①中可以氢氧化钠固体、生石灰;若该现象是由发生化合反应而引起的,那么就是氧化钙和水反应生成了氢氧化钙,则该反应的化学方程式是 CaO+H2O=Ca(OH)2
故答案为:(1)分子是不断运动的 (2)烧杯 ②中有大量气体逸出,烧杯①中的纸花由紫色变为红色;
(3)可能是氢氧化钠(或生石灰等),CaO+H2O=Ca(OH)2
点评:本题难度不大,但综合性较强,解答本题关键掌握分子的基本性质,要考虑气球鼓起的原因是压强增大,可能产生气体或溶于水放出热量,要熟记溶于水放热的常见物质.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目