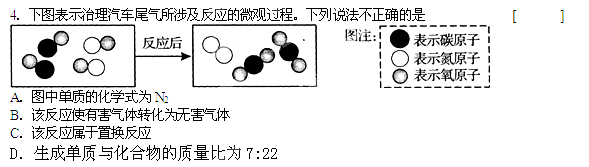
题目内容
某课外活动小组从实验废液中回收银,再检验所得银粉样品中是否含有铁粉:
(1)甲同学用简单的物理方法迅速证了样品中含有铁粉。他的方法是:
(2)乙同学很快拟定了进一步测定样品中银的质量分数的实验步骤:
A.取两药匙样品,加入过量稀硫酸; B.待充分反应后,取出不溶物;C.不溶物经洗涤、干燥后称量,记下其质量。①步骤B中如何判断已充分反应?
②步骤B中主要操作的名称是____________,需要用到的仪器和用品有铁架台(带铁圈)、烧杯、______________、_______________、________________。
③根据乙同学的设计进行实验___________达到目的(填“能”或“不能”),说明理由:
________________________________________________________________________。
(1)用磁铁吸引铁粉(2)①若溶液中不再产生气泡,则已充分反应 ②过滤 漏斗、玻璃棒、滤纸 ③不能 未称量样品的质量。

下表是某种常见金属的部分性质:
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
将该金属投入稀盐酸中,可产生大量的无色气体。根据上述信息回答以下问题:
(1) 试推断该金属可能的一种用途____________________________;
(2) 该金属的活动性比铜__________________________(填“强”或“弱”);
(3) 请自选试剂,设计实验探究该金属与铁的活动性强弱,并完成下表:
| 你的一种猜想 | 验证方法 | 现象 | 结论 |
下表是NaCl、KNO3在不同温度时的溶解度:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
据此数据,判断下列说法错误的是 ( )
A.KNO3和NaCl的溶解度曲线在20℃~30℃温度范围内会相交
B.在60℃时,KNO3的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C.在20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D.从含有少量NaCl的KN03饱和溶液中得到较多的KNO3晶体,通常可采用冷却热饱和溶液的方法
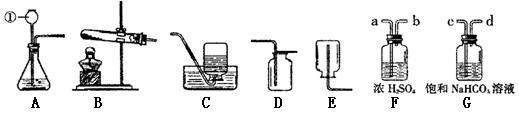 下图是实验室常用的装置。请据图回答:
下图是实验室常用的装置。请据图回答: D.4:1
D.4:1