题目内容
13. 如图是甲、乙两种固体物质的溶解度曲线,回答下列问题.
如图是甲、乙两种固体物质的溶解度曲线,回答下列问题.(1)t1℃时,乙的溶解度大于甲的溶解度(填“大于”或“等于”或“小于”)
(2)把甲物质的不饱和溶液变成饱和溶液,下列有关说法正确的是DE(填字母序号).
A.溶剂的质量一定变小
B.溶质的质量一定不变
C.溶质的质量分数一定变大
D.溶液的质量分数可能不变
E.该饱和溶液还可以溶解其他物质.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,乙的溶解度大于甲的溶解度;
(2)把甲物质的不饱和溶液变成饱和溶液,
A.如果是增加溶质,溶剂的质量不变,故错误;
B.如果是增加溶质,溶质的质量变大,故错误
C.如果是降低温度,溶质的质量分数不变,故错误;
D.如果是降低温度,溶质的质量分数不变,溶液的质量分数可能不变,故正确;
E.该饱和溶液还可以溶解其他物质,饱和溶液中还能溶解其他物质,故正确.
故选:DE.
故答案为:(1)大于;
(2)DE.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
4.根据日常经验和所学的化学知识,判断下列变化属于物理变化的是( )
| A. | 车轮爆胎 | B. | 铁锅生锈 | C. | 粮食酿醋 | D. | 光合作用 |
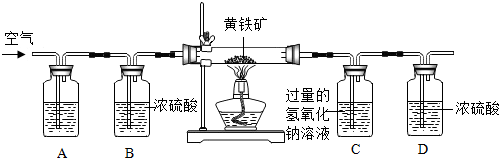
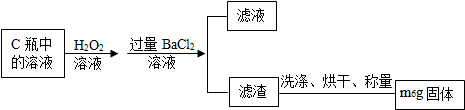
8. “春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量.深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种.某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加人AgNO3溶液测定其浓度.所得数据如图表所示.
“春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量.深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种.某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加人AgNO3溶液测定其浓度.所得数据如图表所示.
(1)生成沉淀的质量a=287.0g.
(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
 “春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量.深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种.某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加人AgNO3溶液测定其浓度.所得数据如图表所示.
“春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量.深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种.某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加人AgNO3溶液测定其浓度.所得数据如图表所示.| 序 号 | 1 | 2 | 3 | 4 | 5 |
| 每次加入AgN03溶液的体积/mL | 100 | 100 | 100 | 100 | 100 |
| 生成沉淀的质量/g | 71.75 | 143.5 | 215.25 | 287.0 | 287.0 |
(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
18.下列记录的实验现象与事实不相符的是( )
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| C. | 能使紫色石蕊试液变红色的物质一定是酸 | |
| D. | 取少量氢氧化钠固体曝露在空气中,氢氧化钠固体表面潮湿并逐渐溶解 |
5.下列实验中利用提供的方案能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去氯化钠溶液中混有的氯化镁 | 先加入过量的NaOH溶液,再过滤 |
| B | 除去CO2中的少量HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| C | 鉴别氢氧化钠和氯化钠固体 | 加适量的水溶解,测量前后温度变化 |
| D | 鉴别稀硫酸和氯化钠溶液 | 滴加酚酞溶液,观察溶液颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
3.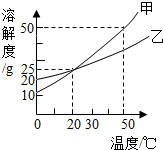 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 20℃时,100g甲溶液中含甲物质的质量为25g | |
| B. | 20℃时,等质量甲、乙饱和溶液中含溶质的质量相等 | |
| C. | 将甲物质从50℃降温到30℃时一定有晶体析出 | |
| D. | 将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为25% |