题目内容
20.小明发现双氧水滴在伤口上会产生大量的气泡,于是他查阅了相关资料:双氧水分解可以用二氧化锰(MnO2)、氧化铁(Fe2O3)等物质作催化剂,对此他展开了探究.【提出问题】氧化铁是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小明以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)
| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | Fe2O3 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
②若实验②比实验①的“待测数据”更小(填“大”或“小”),说明氧化铁能加快氯酸钾的分解.
③将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g红色粉末(Fe2O3),这样做的目的是证明反应后氧化铁的质量没有改变,小明同学认为氧化铁肯定是氯酸钾分解的催化剂,但晓航同学对此提出了异议,晓航同学设计了如下实验:
将第二次精确称量得到的0.5g红色粉末和1.2g氯酸钾混合放入试管中,加热,伸入带火星木条,发现木条很快复燃.
晓航同学这样做目的是证明反应后氧化铁的化学性质没有改变,
【预期结论】氧化铁也能作氯酸钾的催化剂.
【评价设计】你认为小明设计实验③和实验②对比的目的是比较氧化铁和二氧化锰的催化效果;写出实验②反应的符号表达式2KClO3$\stackrel{F{e}_{2}{O}_{3}}{=}$2KCl+3O2↑.
分析 ①运用催化剂的概念和本题的实验目的证明氧化铜能加快氯酸钾的分解解答.
②如果氧化铜能加快氯酸钾的分解速率,实验②比实验①所用时间小.
③根据实验②反应后的固体只有Fe2O3,分析解答.
【评价设计】实验③和实验②对比的目的是探究氧化铜和二氧化锰哪一个催化效果好.
解答 解:
①本题的实验目的证明氧化铜能加快氯酸钾的分解,所以“待测数据”是收集等量氧气所需时间.故答案为:收集等量氧气所需时间.
②如果氧化铜能加快氯酸钾的分解速率,实验②比实验①所用时间小.故答案为:小.
③将实验②反应剩余的固体取出后经洗涤、干燥,再次精确称量得到0.5g红色粉末(Fe2O3),这样做的目的是证明反应后氧化铁的质量没有改变;将第二次精确称量得到的0.5g红色粉末和1.2g氯酸钾混合放入试管中,加热,伸入带火星木条,发现木条很快复燃,这样做目的是证明反应后氧化铁的化学性质没有改变.
【评价设计】实验③和实验②对比的目的是探究氧化铁和二氧化锰哪一个催化效果好,实验②反应的符号表达式2KClO3$\stackrel{F{e}_{2}{O}_{3}}{=}$ 2KCl+3O2↑.
故答案为:【设计实验】①生成等体积氧气所需的时间.②小.
③证明反应后氧化铁的质量没有改变. 证明反应后氧化铁的化学性质没有改变,
【评价设计】比较氧化铁和二氧化锰的催化效果; 2KClO3$\stackrel{F{e}_{2}{O}_{3}}{=}$ 2KCl+3O2↑
点评 考虑催化剂只是改变反应的速率,对反应的生成物及生成物的量都没有影响,本身的质量不变;抓住催化剂的质量反应前后不变和能加快其他物质的化学反应速率这两个性质探究.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
11.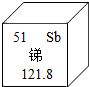 如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
 如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )| A. | 元素属于金属元素 | B. | 锑原子核外有51个电子 | ||
| C. | 锑元素的相对原子质量是121.8g | D. | 锑元素的原子序数为51 |
8.观察和实验是学习化学的重要方式,下列实验现象描述正确的是( )
| A. | 细铁丝在氧气中燃烧,生成黑色固体四氧化三铁 | |
| B. | 镁条在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| C. | 纯净的氢气在空气中安静燃烧,火焰呈蓝紫色 | |
| D. | 木炭在氧气中燃烧,发出明亮的火焰 |
15.如图所示实验操作中正确的是( )
| A. |  | B. |  | C. |  | D. | 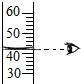 |
12.下列说法不正确的是( )
| A. | 用红磷测定空气中氧气的含量时,燃烧停止冷却至室温,再打开止水夹 | |
| B. | 用排水法收集氧气时,导管口刚有气泡冒出就收集气体 | |
| C. | 硫粉在氧气中燃烧时,集气瓶中放少了水可吸收二氧化硫 | |
| D. | 物质与氧气发生的反应属于氧化反应 |
10.归纳推理是学习化学的重要方法之一.下列有关事实的推理,结论合理的是( )
| A. | H2O和CO2都不能使紫色石蕊变红,把它们混合在一起时却能够使石蕊变红,说明CO2与H2O发生了化学反应 | |
| B. | 在“测定空气中氧气含量”的实验中,集气瓶内水平面上升约1/5,证明了氧气约占空气总质量的1/5 | |
| C. | Al制品的耐腐蚀性比Cu制品强,因此Al的活泼性小于铜 | |
| D. | 盐中含有金属离子和酸根离子,而NH4NO3中没有金属离子,所以不属于盐 |
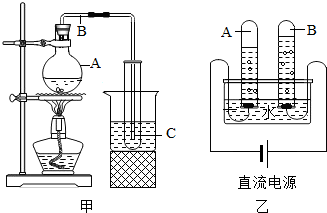 水是一种重要的自然资源,是生活、生成比不可少的物质,请回答下列问题:
水是一种重要的自然资源,是生活、生成比不可少的物质,请回答下列问题: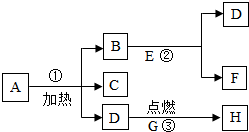 A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变:
A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变: