题目内容
19.取100g溶质质量分数6.8%的过氧化氢溶液与适量二氧化锰制取氧气,当收集到1.6g氧气时,使反应停止,计算:(1)参加反应的过氧化氢的质量.
(2)此时所得的过氧化氢溶液中氧元素的质量分数.(精确到0.1%)
分析 (1)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,依据生成氧气的质量进行分析;
(2)根据过氧化氢溶液中氧元素的质量包括过氧化氢中和水中氧元素的质量进行计算.
解答 解:(1)生成1.6g气体需要该过氧化氢溶液中溶质的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$
x=3.4g
(2)反应前过氧化氢溶液中氧元素的质量为:6.8g×$\frac{32}{34}$+93.2g×$\frac{16}{18}$=89.2g,
所以所得的过氧化氢溶液中氧元素的质量分数为:$\frac{89.2g-1.6g}{100g-1.6g}$×100%=89.1%.
故答案为:(1)3.4g;
(2)89.1%.
点评 本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
9.2015年的诺贝尔生理学或医学奖颁发给了因发现对抗疟疾的青蒿素而获得成功的我国药学家屠呦呦.青蒿素的化学式为C15H22O5,它在湿、热条件下易分解.下列说法不正确的是( )
| A. | 青蒿素属于有机物 | |
| B. | 青蒿素是由碳、氢、氧三种元素组成的 | |
| C. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 | |
| D. | 提取青蒿素不宜在高温下进行 |
7. 如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列有关说法正确的是( )
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列有关说法正确的是( )
 如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列有关说法正确的是( )
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,下列有关说法正确的是( )| A. | 反应前后,溶液的pH不变 | B. | 反应前后,Na+和Cl-的数目不变 | ||
| C. | 反应前后,H+和OH-的数目不变 | D. | 反应前后,H2O的数目不变 |
4. 如图是A、B、C三种固体物质的溶解度曲线.下列分析错误的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列分析错误的是( )
 如图是A、B、C三种固体物质的溶解度曲线.下列分析错误的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列分析错误的是( )| A. | 50℃时,三种物质的溶解度由大到小的顺序是A>B>C | |
| B. | 50℃时,把50gA放入50g水中形成75gA的饱和溶液 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 分别三种的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数是B>C=A |
8.我们吃火锅时经常用到固体酒精.已知酒精燃烧生成二氧化碳和水,下列关于该化学反应的叙述正确的是( )
| A. | 燃烧前后固体酒精的质量没有改变 | |
| B. | 固体酒精减少的质量等于生成的二氧化碳和水的质量 | |
| C. | 固体酒精燃烧后生成物的质量之和等于固体酒精减少的质量与消耗氧气的质量之和 | |
| D. | 燃烧前固体酒精的质量与消耗氧气质量之和等于生成的二氧化碳与水的质量之和 |
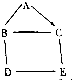
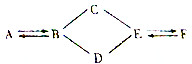 如图A、B、C、D、E、F是切中化学常见的物质,且A、B、C、D、E属于不同类别的物质,C的水溶液呈蓝色,B是年产量最高的金属,A→B的反应可用于冶金工业,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)
如图A、B、C、D、E、F是切中化学常见的物质,且A、B、C、D、E属于不同类别的物质,C的水溶液呈蓝色,B是年产量最高的金属,A→B的反应可用于冶金工业,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)