题目内容
1.写出相对分子质量:(1)NH317
(2)CuSO4•5H2O250.
分析 相对分子质量=相对原子质量与相应原子个数的乘积和,据此解答.
解答 解:(1)NH3的相对分子质量=14+1×3=17;
(2)CuSO4•5H2O的相对分子质量=64+32+16×4+5×(1×2+16)=250;
故答案为:(1)17;(2)250.
点评 本题难度不大,掌握并灵活运用相对分子质量的计算方法即可正确解答本题.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
16.解决问题常面临着方法的选择,面对不同的结果我们应继续探索.为得知硫酸铜晶体中结晶水的质量分数,小柯与小妍分别采取了以下方法:
请你分析:
(1)请你在表格中补充完整小妍同学的计算过程.
(2)由表中数据可得,小柯同学测得硫酸铜晶体中结晶水的质量分数是44%.
(3)比较小柯实验测得值与小妍理论计算所得值之间的误差,造成这种误差的原因可能有(填写字母)AD.
A.加热前称量时容器未完全干燥 B.最后两次加热后质量相差较大(大于0.1g)
C.加热后容器未放入干燥器中冷却 D.加热过程中有少量溅失.
| 小柯:实验测定法 | 小妍:理论计算法 | |||||||||
称取一定量研细的硫酸铜晶体倒在坩埚里,用小火加热至固体全部变成白色,再反复干燥和称量后称得粉状物的质量不再变化.得到以下数据:
| 解:根据硫酸铜晶体的化学式计算硫酸铜中结晶水的质量分数 | |||||||||
(1)请你在表格中补充完整小妍同学的计算过程.
(2)由表中数据可得,小柯同学测得硫酸铜晶体中结晶水的质量分数是44%.
(3)比较小柯实验测得值与小妍理论计算所得值之间的误差,造成这种误差的原因可能有(填写字母)AD.
A.加热前称量时容器未完全干燥 B.最后两次加热后质量相差较大(大于0.1g)
C.加热后容器未放入干燥器中冷却 D.加热过程中有少量溅失.
6.关于质量守恒定律,下列叙述中正确的是( )
| A. | 一切化学反应都遵从质量守恒定律 | |
| B. | 煤燃烧化为灰烬,该反应不符合质量守恒定律 | |
| C. | 质量守恒定律只适用于有气体或固体生成的化学反应 | |
| D. | 24克镁在空气中完全燃烧生成40克氧化镁,实际消耗空气质量为16克 |
10.在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:溶液甲蒸发5g水无晶体析出得到溶液乙,溶液乙蒸发5g水析出2g晶体得到溶液丙.下列结论正确的是( )
| A. | 溶液甲可能是饱和溶液 | |
| B. | 溶液乙和溶液丙中的溶质质量分数可能相等 | |
| C. | 溶液乙一定是饱和溶液 | |
| D. | 溶液丙若再蒸发5g水,析出的晶体一定小于2g |
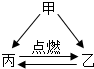 甲、乙、丙是初中化学中常见的三种不同类别的物质,其中乙是水,它们之间的转化关系如图所示.“→”表示由一种物质转化成另一种物质(图中部分反应条件及物质略去).
甲、乙、丙是初中化学中常见的三种不同类别的物质,其中乙是水,它们之间的转化关系如图所示.“→”表示由一种物质转化成另一种物质(图中部分反应条件及物质略去).