题目内容
11.化学是一门以实验为基础的学科.根据下图,回答问题.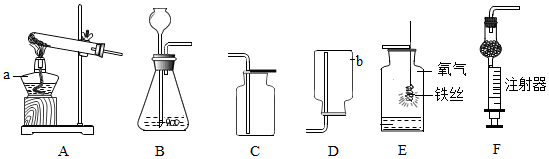
(1)仪器a的名称是酒精灯,仪器b的名称是集气瓶
(2)实验室用过氧化氢和二氧化锰制取氧气,选用的发生装置是B(填字母序号),该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰的作用为催化作用.装置E中,铁丝与氧气反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,选用的收集装置是C(填字母序号).制取二氧化碳时,用装置F替代装置B的优点是可以控制液体的滴加速率.
(4)氨气是一种无色、有强烈刺激性臭味的气体,极易溶于水.水溶液呈碱性,能使无色酚酞试液变红.实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气.某兴趣小组的同学设计如下图G~J所示装置对氨气的制取、性质进行探究.
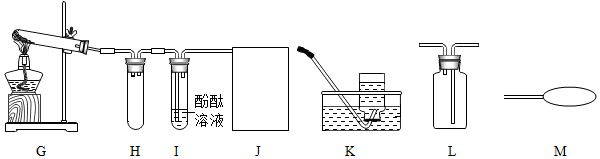
①装置H的作用是防止液体倒流入装置G中,使试管炸裂,
②根据氨气的性质,J处应选择的最佳收集装置为M.(填“K”、“L”或“M”)
分析 (1)根据实验室常用仪器解答;
(2)根据通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;根据铁与氧气反应生成四氧化三铁解答;
(3)根据实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大解答;
(4)根据实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气;制取气体主要看反应物的状态和反应条件;收集气体看气体的密度与水溶性;浓硫酸具有吸水性,可以做干燥剂.
解答 解:(1)根据实验室常用仪器可知:a酒精灯;b集气瓶;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;实验室用过氧化氢制取氧气不需要加热,应该用B装置作为发生装置;其中二氧化锰的作用为催化作用;铁与氧气反应生成四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;二氧化碳能够溶于水,不能用排水法收集,二氧化碳的密度比空气大,可以用向上排空气法收集,即用C装置收集;注射器可以控制液体的滴加速率,故制取二氧化碳时,用装置F替代装置B的优点是可以控制液体的滴加速率;
(4)①由于氨气易溶于水,装置H的作用是防止液体倒流入装置G中,使试管炸裂;
②氨气是一种无色、有强烈刺激性臭味的气体,为防止氨气跑到空气中去,J处应选择的最佳收集装置为M.
故答案为:
(1)a酒精灯;b集气瓶;
(2)B;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.催化作用;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;C;可以控制液体的滴加速率;
(4)①防止液体倒流入装置G中,使试管炸裂;②M.
点评 制取装置包括加热和不需加热两种,实验室制取CO2用的药品是石灰石或大理石与稀盐酸,石灰石或大理石的主要成分是碳酸钙,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.

 53随堂测系列答案
53随堂测系列答案| A. | 分子是可分的 | B. | 分子之间有间隔 | ||
| C. | 分子在不断地运动 | D. | 分子很小 |
| A. | 二氧化氮 | B. | 二氧化硫 | C. | 氮气 | D. | 沙尘暴 |
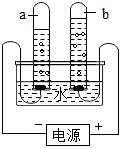 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: