题目内容
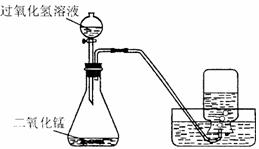
(5分)如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。

|
|
气体发生装置内物质的总质量 |
|
反应前 |
35.6 |
|
反应后 |
34.8 |
(l)反应中二氧化锰的作用是 。
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。
(1)加快过氧化氢分解的速率(1分)
(2)0.8(1分)
(3)解:设参加反应的过氧化氢的质量为X
2H2O2 2H2O + O2↑ (1分)
2H2O + O2↑ (1分)
68 32
X 0.8g (1分)
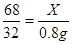 X=1.7g
(1分)
X=1.7g
(1分)
答:参加反应的过氧化氢的质量为1.7g
【解析】
试题分析:1、二氧化锰是催化剂,在反应中起催化作用;
2、由题意可知,整个装置内物质减少的质量应为过氧化氢分解产生氧气的质量,故反应生成氧气的质量为:35.6-34.8=0.8克;
3、氧气由过氧化氢分解生成,根据化学方程式计算可得过氧化氢的质量。
解:设参加反应的过氧化氢的质量为X
2H2O2 2H2O + O2↑ (1分)
2H2O + O2↑ (1分)
68 32
X 0.8g (1分)
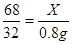 X=1.7g
(1分)
X=1.7g
(1分)
答:参加反应的过氧化氢的质量为1.7g
考点:催化剂;根据化学方程式计算。
点评:催化剂具有催化作用,能改变化学反应的速率,而其本身质量和化学性质在反应前后保持不变;根据化学方程式计算时,要注意解题的步骤。

 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案(9分)⑴化学是一门以实验为基础的学科,取用块状药品通常用 ,取用一定量的液体时需要 ,实验结束时要洗涤仪器,玻璃仪器洗涤干净的标志是 。
(2)在“ 氧气的制取和性质”实验中,某同学取一段纱窗网上还能任意弯曲的细铁丝,在新制的氧气中做“铁丝燃烧”的实验。结果没有观察到“火星四射”的现象,请分析此实验失败的原因 (写一种);经过改进后实验成功了,其反应的符号表达式 。实验时要在集气瓶底部铺一层细沙或装少量水的原因是 。
(3)如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。
| | 气体发生装置内物质的总质量(g) |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
②反应生成氧气的质量为 g(结果精确到0. 1 g)。
(3分)如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。

|
|
气体发生装置内物质的总质量 |
|
反应前 |
35.6 g |
|
反应后 |
34. 8 g |
(l)实验中检查该装置气密性的方法是________________________________ 。
(2)实验中集气瓶收集满氧气的现象是________________________________。
(3)反应生成氧气的质量为:_______________ g 。
如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。
|
| 气体发生装置内物质的总质量 |
| 反应前 | 35.6 g |
| 反应后 | 34. 8 g |
(l)实验中检查该装置气密性的方法是________________________________ 。
(2)实验中集气瓶收集满氧气的现象是________________________________。
(3)反应生成氧气的质量为:_______________ g 。
 (1)化学是一门以实验为基础的学科,取用块状药品通常用
(1)化学是一门以实验为基础的学科,取用块状药品通常用