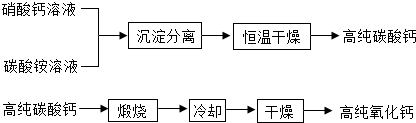
题目内容
 碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如图所示.另取相同质量的该混合物溶于水得到106.6g溶液,向该溶液中加入100g 7.3% 的稀盐酸,恰好完全反应.(已知:2NaHCO3
碳酸钠和碳酸氢钠的固体混合物充分加热至恒重,其质量变化如图所示.另取相同质量的该混合物溶于水得到106.6g溶液,向该溶液中加入100g 7.3% 的稀盐酸,恰好完全反应.(已知:2NaHCO3
| ||
(1)混合物与盐酸反应生成二氧化碳的质量.
(2)所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据图中数据可以判断碳酸氢钠分解生成水和二氧化碳的质量,进一步可以计算碳酸氢钠和碳酸钠的质量;
根据碳酸钠、碳酸氢钠的质量可以计算混合物与盐酸反应生成二氧化碳的质量,进一步可以计算所得溶液中溶质的质量分数.
根据碳酸钠、碳酸氢钠的质量可以计算混合物与盐酸反应生成二氧化碳的质量,进一步可以计算所得溶液中溶质的质量分数.
解答:解:(1)设碳酸钠和稀盐酸反应生成二氧化碳的质量为x,生成的氯化钠的质量为m,碳酸氢钠和稀盐酸反应生成二氧化碳的质量为y,生成的氯化钠的质量为n,碳酸氢钠的质量为z,
由图中数据可知,碳酸氢钠受热分解生成水和二氧化碳的质量为:13.7g-10.6g=3.1g,
2NaHCO3
Na2CO3+CO2↑+H2O,
168 62
z 3.1g
=
,
z=8.4g,
碳酸钠的质量为:13.7g-8.4g=5.3g,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaHCO3+HCl═NaCl+H2O+CO2↑,
106 117 44 84 58.5 44
5.3g m x 8.4g n y
=
=
,
=
=
,
m=5.85g,x=2.2g,n=5.85g,y=4.4g,
混合物与盐酸反应生成二氧化碳的质量为:2.2g+4.4g=6.6g,
答:生成二氧化碳的质量为6.6g.
(2)所得溶液质量为:106.6g+100g-6.6g=200g,
溶质的质量分数为:
×100%=5.85%,
答:所得溶液中溶质的质量分数为5.85%.
由图中数据可知,碳酸氢钠受热分解生成水和二氧化碳的质量为:13.7g-10.6g=3.1g,
2NaHCO3
| ||
168 62
z 3.1g
| 168 |
| z |
| 62 |
| 3.1g |
z=8.4g,
碳酸钠的质量为:13.7g-8.4g=5.3g,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaHCO3+HCl═NaCl+H2O+CO2↑,
106 117 44 84 58.5 44
5.3g m x 8.4g n y
| 106 |
| 5.3g |
| 117 |
| m |
| 44 |
| x |
| 84 |
| 8.4g |
| 58.5 |
| n |
| 44 |
| y |
m=5.85g,x=2.2g,n=5.85g,y=4.4g,
混合物与盐酸反应生成二氧化碳的质量为:2.2g+4.4g=6.6g,
答:生成二氧化碳的质量为6.6g.
(2)所得溶液质量为:106.6g+100g-6.6g=200g,
溶质的质量分数为:
| 5.85g+5.85g |
| 200g |
答:所得溶液中溶质的质量分数为5.85%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
下列物质中属于纯净物的是( )
| A、生理盐水 | B、消毒酒精 |
| C、碘酒 | D、冰水混合物 |
下列方框中,符合2N2意义的示意图是(其中 表示氮原子)( )
表示氮原子)( )
 表示氮原子)( )
表示氮原子)( )A、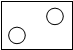 |
B、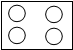 |
C、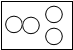 |
D、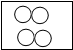 |
常温常压下,10mL某气态物质含有1.04×1020个分子,而在这些分子里有含有3.12×1020个原子,则该物质属于( )
| A、单质 | B、化合物 |
| C、混合物 | D、无法确定类别 |
“酒驾”是当前热门话题之一.喝酒不开车,开车不喝酒.酒后驾驶是一种违法行为,交巡警检查驾驶员是否饮酒的仪器里装有重铬酸钾(化学式为K2Cr2O7).下列关于重铬酸钾的说法正确的是( )
| A、它是氧化物 |
| B、重铬酸钾是由2个钾原子、2个铬原子、7个氧原子构成 |
| C、含有K、Cr、O三种元素 |
| D、钾、铬、氧三种元素的质量比为2:2:7 |
下列各组物质中,氯元素化合价相同的一组是( )
| A、Cl2 HCl |
| B、NaCl HClO |
| C、ClO2 NaClO2 |
| D、NaClO HClO |