题目内容
7.粗盐中含有MgCl、CaCl2等杂质,工业提纯粗盐的工艺流程如图所示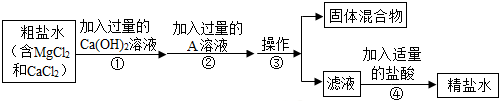
(1)步骤①反应的化学方程式为Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓
(2)A的化学式是Na2CO3固体混合物的主要成分是Mg(OH)2沉淀和CaCO3沉淀
(3)步骤④加入适量盐酸的目的是除去滤液中的Na2CO3和NaOH.
分析 (1)Ca(OH)2溶液只能与粗盐水中的MgCl2反应,据此写出化学反应式;
(2)根据Ca(OH)2可除去MgCl2,Na2CO3可除去CaCl2分析;
(3)经过①②后,要进行过滤实验除去沉淀,加入适量的盐酸可以除去滤液中多余的Na2CO3和NaOH.
解答 解:(1)Ca(OH)2溶液只能与粗盐水中的MgCl2反应,化学反应方程式是:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;故答案为:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓.
(2)Na2CO3可除去CaCl2和过量的氢氧化钙;经过①②后,生成沉淀,要进行过滤实验除去沉淀,所以要进行过滤,过滤出的固体混合物中有步骤①生成的氢氧化镁沉淀和步骤②生成的碳酸钙沉淀;故答案为:Na2CO3;Mg(OH)2沉淀和CaCO3沉淀;
(3)经过过滤后,滤液中还有加入过量的Na2CO3和生成的NaOH,因此要加入盐酸,把Na2CO3和NaOH除去,转化为氯化钠;故答案为:NaOH.
点评 粗盐提纯是经常考查的内容,其中要涉及到化学方程式的书写、过滤操作、杂质的除去等内容,需要同学们对此内容了然于心.

练习册系列答案
相关题目
17.肉毒碱(C7H15NO3)被认为是“最佳减肥营养素”.关于它的说法正确的是( )
| A. | 质量分数最大的元素是氧元素 | |
| B. | 肉毒碱中含有臭氧 | |
| C. | 肉毒碱中碳元素和氧元素的质量比为7:3 | |
| D. | 它是一种有机化合物 |
18.下列食物中,富含维生素的是( )
| A. | 苹果 | B. | 牛奶 | C. | 鱼肉 | D. | 米饭 |
12.下列制取Fe2(SO4)3溶液的方案中,从反应原理和产物纯度考虑最佳的是( )
| A. | 过量的Fe粉与稀硫酸反应,过滤 | B. | 过量的Fe粉与CuSO4溶液反应,过滤 | ||
| C. | 过量的稀硫酸与Fe2O3反应 | D. | 过量的Fe2O3与稀硫酸反应,过滤 |
17.自热米饭是一种快餐食品.请根据图中信息回答下列问题:
自热米饭的营养成分
(1)自热米饭的营养成分中,主要提供能量的是糖类,构成细胞的基础物质是蛋白质,油脂不是(填“是”或“不是”) 高分子化合物;标签中的“钙130mg”,这里的“钙”是指A(填编号).
A.元素 B.原子 C.分子 D.离子
(2)菜肴包的包装材料是铝箔.铝可以压制成铝箔,说明铝具有良好的延展性.铝不是有害元素,但它是非必需元素,经常摄入铝会造成老年痴呆症,请举一例说明生活中如何避免摄入较多量的铝元素.尽量少用铝制品炒菜、煮饭.
(3)该自热米饭是利用发热包中的生石灰与水反应作为热源,其化学方程式为CaO+H2O═Ca(OH)2,该反应为放热反应(填“放热”或“吸热”).

自热米饭的营养成分
| 营养素 | 每份含量 |
| 蛋白质 | 29.6g |
| 油脂 | 23.5g |
| 糖类 | 104.7g |
| 钠 | 814mg |
| 钙 | 130mg |
A.元素 B.原子 C.分子 D.离子
(2)菜肴包的包装材料是铝箔.铝可以压制成铝箔,说明铝具有良好的延展性.铝不是有害元素,但它是非必需元素,经常摄入铝会造成老年痴呆症,请举一例说明生活中如何避免摄入较多量的铝元素.尽量少用铝制品炒菜、煮饭.
(3)该自热米饭是利用发热包中的生石灰与水反应作为热源,其化学方程式为CaO+H2O═Ca(OH)2,该反应为放热反应(填“放热”或“吸热”).

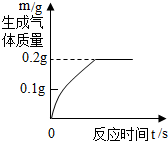 将6.8g含杂质的锌粒,加入到盛有50.0g稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应)正好完全反应,生成气体与时间关系如图,过滤得溶液质量为56.6g.试计算:
将6.8g含杂质的锌粒,加入到盛有50.0g稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应)正好完全反应,生成气体与时间关系如图,过滤得溶液质量为56.6g.试计算:
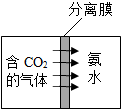 通过化学学习,同学们对物质的组成和结构有了一定的了解.
通过化学学习,同学们对物质的组成和结构有了一定的了解. ,则X=8.
,则X=8.