题目内容
某地质勘探研究所欲对某铝土矿的样品中氧化铝的纯度进行测量(假设其他成分不含铝元素,且不溶于水,也不与酸反应),请回答下列问题:
(1)配制100g的质量分数为19.6%的稀硫酸,需98%的浓硫酸的质量是
(2)氧化铝跟稀硫酸反应的化学方程式是
(3)若将铝土矿样品制成粉末,取5g粉末与60g的19.6%的稀硫酸恰好充分反应后,过滤.向滤渣中加入稀硫酸无变化;向滤液中加入铝土矿粉末也不溶解.则求解5g铝土矿样品中氧化铝(x)的比例式为
(4)此铝土矿样品中氧化铝的质量分数为 ;
(5)若将(3)反应后得到的滤液蒸发掉9.36g水后,仍为不饱和溶液,则所得溶液中溶质的质量分数为 .
(6)某大型金属冶炼厂采用这种铝土矿电解制铝块,生产过程中铝元素损耗12%.要生产4.8万吨含杂质1%铝块,则至少需购买这种铝土矿 万吨.
(1)配制100g的质量分数为19.6%的稀硫酸,需98%的浓硫酸的质量是
(2)氧化铝跟稀硫酸反应的化学方程式是
(3)若将铝土矿样品制成粉末,取5g粉末与60g的19.6%的稀硫酸恰好充分反应后,过滤.向滤渣中加入稀硫酸无变化;向滤液中加入铝土矿粉末也不溶解.则求解5g铝土矿样品中氧化铝(x)的比例式为
(4)此铝土矿样品中氧化铝的质量分数为
(5)若将(3)反应后得到的滤液蒸发掉9.36g水后,仍为不饱和溶液,则所得溶液中溶质的质量分数为
(6)某大型金属冶炼厂采用这种铝土矿电解制铝块,生产过程中铝元素损耗12%.要生产4.8万吨含杂质1%铝块,则至少需购买这种铝土矿
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:有关化学方程式的计算
分析:(1)中可看作是溶液稀释问题的计算,根据稀释前后溶液中溶质的质量不变,列出等式即可求解;
(2)(3)中要求会写氧化铝与盐酸反应的化学方程式,然后根据化学方程式即可列出比例式;
(4)中根据前一步求出的铝的质量,用氧化铝的质量和样品的质量比便可求出样品中氧化铝的质量分数;
(5)中,根据化学方程式先求出生成的硫酸铝的质量和氢气的质量,然后根据质量守恒定律便可求出反应后所得溶液的总质量,这样便可轻松求解.
(6)根据铝元素守恒进行解答.
(2)(3)中要求会写氧化铝与盐酸反应的化学方程式,然后根据化学方程式即可列出比例式;
(4)中根据前一步求出的铝的质量,用氧化铝的质量和样品的质量比便可求出样品中氧化铝的质量分数;
(5)中,根据化学方程式先求出生成的硫酸铝的质量和氢气的质量,然后根据质量守恒定律便可求出反应后所得溶液的总质量,这样便可轻松求解.
(6)根据铝元素守恒进行解答.
解答:解:(1)设需要浓硫酸的质量为X.
100g×19.6%=X?98%
X=20g
故答案为:20g;
(2)书写化学方程式时要注意铝元素的化合价为+3价,氧化铝和硫酸反应生成硫酸铝和水,反应的化学方程式是Al2O3+3H2SO4═Al2(SO4)3+3H2O;
故答案为:Al2O3+3H2SO4═Al2(SO4)3+3H2O;
(3)设5g样品中氧化铝的质量为x.完全反应生成硫酸铝的质量为y.
Al2O3+3H2SO4═Al2(SO4)3+3H2O
102 294 342
x 60g×19.6% y
=
x=4.08g
=
y=13.68g
故答案为:
=
;
(4)此铝土矿样品中氧化铝的质量分数为=
×100%=81.6%
故答案为:81.6%;
(5)所得溶液中溶质的质量分数=
×100%=25%;故答案为25%;
(6)设需要这样中的铝土矿的质量为z.
z×81.6%×
×100%×(1-12%)=4.8万吨×(1-1%)
z=125万吨
故答案为:125.
100g×19.6%=X?98%
X=20g
故答案为:20g;
(2)书写化学方程式时要注意铝元素的化合价为+3价,氧化铝和硫酸反应生成硫酸铝和水,反应的化学方程式是Al2O3+3H2SO4═Al2(SO4)3+3H2O;
故答案为:Al2O3+3H2SO4═Al2(SO4)3+3H2O;
(3)设5g样品中氧化铝的质量为x.完全反应生成硫酸铝的质量为y.
Al2O3+3H2SO4═Al2(SO4)3+3H2O
102 294 342
x 60g×19.6% y
| 102 |
| x |
| 294 |
| 60g×19.6% |
x=4.08g
| 294 |
| 60g×19.6% |
| 342 |
| y |
y=13.68g
故答案为:
| 102 |
| x |
| 294 |
| 60g×19.6% |
(4)此铝土矿样品中氧化铝的质量分数为=
| 4.08g |
| 5g |
故答案为:81.6%;
(5)所得溶液中溶质的质量分数=
| 13.68g |
| 4.08g+60g-9.36g |
(6)设需要这样中的铝土矿的质量为z.
z×81.6%×
| 54 |
| 102 |
z=125万吨
故答案为:125.
点评:本题考查了学生对:金属氧化物与酸反应的化学方程式的掌握以及有关溶液中溶质的判断,反应后所得溶液的质量求法的掌握,反应后所得溶液质量的求法利用质量守恒定律求解是最简单的一种方法.该题难度比较大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
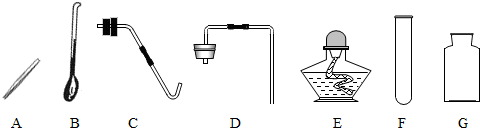
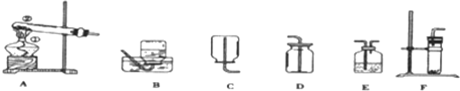
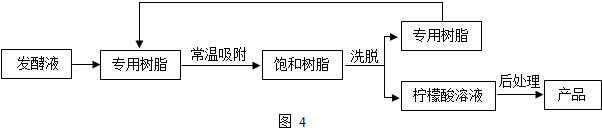
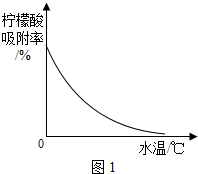 柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题:
柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题: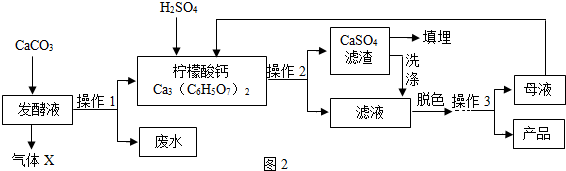
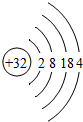 ,请根据结构示意图回答下列问题:
,请根据结构示意图回答下列问题: