题目内容
19.如图是某学校实验小组的同学的实验过程,请你根据如图所示提供的数据计算.
求:(1)求该样品中碳酸钠的质量分数;
(2)求反应后溶液的溶质质量分数;
(3)将所得不饱和溶液配置成20%的氯化钠溶液需要向溶液中加入氯化钠多少克?(精确到0.1g).
分析 (1)根据质量守恒定律计算生成二氧化碳的质量,依据二氧化碳的质量和化学方程式进行计算相关的数据;
(2)根据题中的数据计算反应后溶液和溶质的质量,然后计算溶质的质量分数;
(3)根据溶液配制前后溶质的质量不变进行分析.
解答 解:(1)生成二氧化碳的质量为20g+100g+95.4g-211g=4.4g;
设样品中碳酸钠的质量为x,恰好完全反应后生成的氯化钠质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{4.4g}$
x=10.6g
y=11.7g
所以样品中碳酸钠的质量分数为$\frac{10.6g}{20g}$×100%=53%;
(2)反应后溶液中溶质的质量为20g-10.6g+11.7g=21.1g,
所得不饱和溶液中溶质的质量分数为$\frac{21.1g}{211g}$×100%=10%;
(3)若将所得不饱和溶液配制成20%的氯化钠溶液,需要向溶液中加入氯化钠的质量为z
$\frac{21.1g+z}{211g+z}$×100%=20%
z=26.4g
故答案为:(1)53%;
(2)10%;
(3)26.7g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
9.家庭生活中处处有物质的变化,以下属于物理变化的是( )
| A. | 鲜牛奶变质 | B. | 酵母粉发酵 | C. | 洁厕精除垢 | D. | 钢丝球刷碗 |
11.日常生活中我们食用的加碘食盐中的“碘”指的是( )
| A. | 分子 | B. | 原子 | C. | 元素 | D. | 单质 |
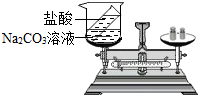 验证质量定律:有人设计如图所示的实验来验证质量守恒定律,把装有稀盐酸的小试管放入盛有碳酸钠溶液的烧杯中,将将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡.
验证质量定律:有人设计如图所示的实验来验证质量守恒定律,把装有稀盐酸的小试管放入盛有碳酸钠溶液的烧杯中,将将烧杯放到托盘天平上,用砝码平衡.取下烧杯并将其倾斜,使两种溶液混合反应,再把烧杯放到天平上,观察天平是否平衡.